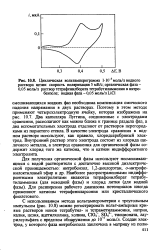
Рабочий диапазон - потенциал
Cтраница 1
Рабочий диапазон потенциалов в данной системе зависит от материала эчектрода, электролита фона, температуры [231] и растворителя. В данном разделе рассматривается только влияние растворителя. [1]
Рабочий диапазон потенциалов в катодной области довольно ограничен из-за выделения водорода, тогда как в анодной области можно достичь значений потенциала около - j - 2 5 В ( отн. КЭ) В качестве электролита фона можно использовать фторид натрия или калия, добавление этих солей снижает протонирующую способность растворителя. [2]
ДМФА имеет удобный рабочий диапазон потенциалов в катодной области ( сравнимый с ацетонитричом), но в анодной области этот диапазон менее удобен. В присутствии неорганических ионов их разряд является катодной лимитирующей реакцией; если же в растворе находятся ионы тетраалкиламмония, катодной лимитирующей реакцией может быть как восстановление растворителя, так н разряд катиона. Анодная лимитирующая реакция па платиновом электроде - окисление ДМФА, включающее отрыв электрона от атома азота. [3]
Для расширения рабочего диапазона потенциалов иногда применяют катионы тетрафениларсония или кристаллического фиолетового. [5]
 |
Схема ячейки для измерений на границе раздела двух несмешивающихся растворов электролитов. [6] |
При этом границы рабочего диапазона потенциалов определяются значениями потенциалов, при которых ионы В ] и Af переходят из органической фазы в водную фазу, а ионы В2 и А2 - - в обратном направлении. [7]
Если же в одном из растворителей наряду с ионами В /, В2, АГ, А2 - содержится ион X, который присутствует в значительно меньшей концентрации, чем остальные ионы, и имеет значение АЕ в пределах рабочего диапазона потенциалов, то при наложении соответствующей разности потенциалов ион л будет переходить из одной фазы в другую. [8]
Электроды сравнения, используемые в воде, например Hg / Hg и Ag / Ag, в большинстве случаев пригодны и для метанола. Рабочий диапазон потенциалов для препаративного электролиза приблизительно тот же, что и в воде, по метанол менее удобен для электроаналитическнх исследований. [9]
Используемые для проведения окислительно-восстановительных реакций растворители должны быть устойчивы к действию окислителей и восстановителей. Рабочий диапазон потенциалов растворителя должен быть достаточно велик. [10]
ГМФТА, подобно ДМФА, не пригоден для анодных реакций из-за легкого окнслення атомов азота. Для катодных реакций рабочий диапазон потенциалов в присутствии LiCl достигает значения, при котором начинается переход электронов в раствор. [11]
Источниками помех в вольтамперометрии часто являются присутствующие в растворе посторонние электроактивные вещества, например растворенный кислород. Кроме того, на краях рабочего диапазона потенциалов обычно наблюдаются помехи, обусловленные вступлением в электрохимическую реакцию материала индикаторного электрода или фонового электролита. В случаях, когда фарадеевские токи определяемых компонентов частично перекрываются, они также оказываются помехой по отношению друг к другу, в особенности по отношению к компоненту с меньшей концентрацией, имеющему соответственно меньший ток. При этом, как и в спектрометрии, актуальна проблема повышения разрешающей способности вольтамперометрических методов. [12]
Наряду с электролитом ячейки исключительно большое значение имеет выбор растворителя. При выборе растворителя следует учитывать такие факторы, как протонодонорная способность, рабочий диапазон потенциалов, склонность к образованию ионных пар, диэлектрическая проницаемость, способность растворять электролиты и исходные вещества, летучесть, вязкость, токсичность и др. В основном применяются водные среды, в которых растворителем служит вода. [13]
Из всех спиртов лишь метанол широко используется как растворитель для проведения электроокисления. Он имеет довольно высокую диэлектрическую проницаемость, растворяет большинство электролитов и имеет умеренный рабочий диапазон потенциала в анодной области. Метанол и его сопряженное основание ( метилат-ион) взаимодействуют с анодно-гене-рированными катионными частицами ( см. также разд. При проведении анодного метоксилирования в метаноле в присутствии метилат-иона при таком значении потенциала, когда одновременно может происходить разряд аниона электролита и окисление органического субстрата, возможна реализация двух механизмов: 1) взаимодействие катион-радикал - метилат-ион и 2) сочетание катион-радикал - метокси-радикал. [14]
Среди материалов для изготовления инертных электродов наиболее предпочтительны ртуть и благородные металлы. Преимущество электродов из благородных металлов в том, что при прохождении электрического тока они не вступают в химические реакции с компонентами электролита, и, следовательно, рабочий диапазон потенциалов поляризации электрода зависит только от состава раствора. [15]
Страницы: 1 2