Химическое представление
Cтраница 1
Химические представления исключают возможность бесконечно большой - скорости реакции, даже в случае серебра, вовсе лишенного пленки. [1]
Наши химические представления об асфальтах весьма ограниченны. Повидимому асфальты и смолы содержатся в минеральных маслах в коллоидальном состоянии, обладая в то же время весьма сложной структурой. [2]
Система химических представлений, принятых на этом съезде, составляет основу так называемой атомно-молекулярной теории, основные положения которой нужно знать очень хорошо. [3]
Такими химическими представлениями можно прекрасно объяснить и вышеуказанное правило значности, согласно которому с увеличением валентности коагулирующего иона его осаждающая возрастает. [4]
В классическом химическом представлении рдсдаоритель не должен оказывать воздействие на количество свободных радикалов в изучаемом объекте при растворении. Однако уже первая работа Гомберга [1] опровергает такое утверждение. [5]
Подчиняя же химические представления закону замещений, мы предугадываем металепсию, как частный случай общего закона. Не должно, однако, упускать из вида, что во всех продуктах металепсии хлор более или менее реагирует иначе, чем хлор в хлористых металлах. Так, в растворе обычных МС1 растворимые соли серебра AgX тотчас дают AgCl - j - MX, а с продуктами металепсии обыкновенно подобная реакция идет медленно. Не входя в рассмотрение скоростей реагирования ( это рассматривается теоретическою химиею), замечу только, что в так называемых комплексных соединениях ( гл. AgX, или действует медленно, напоминая этим хлор металептический. Отношения этого последнего свойства в наше время нельзя считать достаточно выясненными, над ними работают многие и они представляют большой интерес - особого рода. [6]
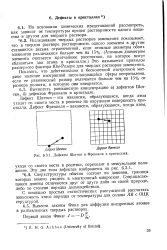 |
Дефекты Шоттки и Френкеля в кристаллах. [7] |
На основании химических представлений рассмотреть, как зависит от температуры предел растворимости одного вещества в другом для твердого раствора. [8]
На основании современных химических представлений эти авторы пришли к выводу, что цинковые соли ксантогеновой и дитио-карбаминовых кислот играют роль переносчиков серы. [9]
Развиваемая им теория сочетает физические и химические представления о природе растворов. На основании статистической теории пока не представляется возможным определить электростатическое слагаемое изобарного потенциала концентрированных растворов, поэтому Г. И. Микулин ищет его, исходя из твердо установленных эмпирических закономерностей. Сочетая это положение с представлением о гидратации ионов как о процессе образования в растворе комплексных соединений, аналогичных ионам аквасолей и характеризуемых целыми гидратными числами и константами нестойкости, и используя закон действующих масс, Г. И. Микулин получил уравнения для вычислений коэффициентов активности электролита и давлений паров воды. Эти формулы в дальнейшем были распространены на смешанные растворы и была рассчитана совместная растворимость двух солей по опытным данным о коэффициентах активности бинарных растворов этих солей. Для системы Na, К / СГ, NO3 - H20 при 25 С было получено хорошее совпадение с опытными данными. Так как количественные теории электролитных растворов развиваются очень медленно и у нас, и за рубежом, эти исследования Г. И. Микулина следует считать весьма плодотворными и перспективными. [10]
Развиваемая им теория сочетает физические и химические представления о природе растворов. На основании статистической теории пока не представляется возможным определить электростатическое слагаемое изобарного потенциала концентрированных растворов, поэтому Г. И. Микулин ищет его, исходя из твердо установленных эмпирических закономерностей. Сочетая это положение с представлением о гидратации ионов как о процессе образования в растворе комплексных соединений, аналогичных ионам аквасолей и характеризуемых целыми гидратными числами и константами нестойкости, и используя закон действующих масс, Г. И. Микулин получил уравнения для вычислений коэффициентов активности электролита и давлений паров воды. Эти формулы в дальнейшем были распространены на смешанные растворы и была рассчитана совместная растворимость двух солей по опытным данным о коэффициентах активности бинарных растворов этих солей. [11]
Бутлерова и М. Д. Львова в формировании химических представлений Фаворского очень велика, и Алексей Евграфович с благодарностью и часто указывал на это в воспоминаниях о своих учителях. [12]
Это и было началом происхождения химических представлений, на этом положено основание тому закону замещения, который выше был изложен. [13]
Мысль Менделеева билась в тисках химических представлений XIX века. Периодический закон, это понимал и сам Менделеев, явно не вмещался в рамки общепринятых, устоявшихся, тысячекратно проверенных опытом формул и положений. [14]
Что касается непрерывности процесса, то химические представления ему не противоречат, и автором было специально доказано, что в каждой точке непрерывной кривой образуются соединения постоянного состава, но в концентрации, соответствующей условию равновесия. [15]
Страницы: 1 2 3 4