Химическое представление
Cтраница 2
Все эти положения, наряду с общими структурными химическими представлениями, и могут приниматься во внимание при интерпретации зависимости электродных свойств стекол от их химического состава на основ. [16]
Все эти положения, наряду с общими структурными химическими представлениями, и могут приниматься во внимание при интерпретации зависимости электродных свойств стекол от их химического состава на основе представлений обобщенной теории. [17]
Вернер определил структуру комплексов, исходя из химических представлений, но после разработки в 20 - е годы нашего столетия рентгенографического анализа и У. Л. Брэгги доказали, что кристаллическая структура типичной комплексной соли - хлорида гек-саамминкобальта ( Ш) [ Со ( МН3) б ] С13 совпадает с представлениями Вернера и является правильным октаэдром. Позже была установлена кристаллическая структура очень многих комплексных солей. В табл. 4.30 приведены примеры типичной пространственной конфигурации комплексных солей. [18]
Таким образом, было положено начало развитию химических представлений об образовании коллоидных растворов, утвердившихся в современной коллоидной химии, а вывод А. В. Думанского о том, что коллоидный раствор можно рассматривать как суспендированные в воде частички, оболочками которых является химический состав коллоида, теперь общепризнан. Не менее важны результата его ра5от по исследованию роли комплексообразования при формировании частиц дисперсной фазы, как промежуточной стадии образования коллоидно-дисперсной системы. [19]
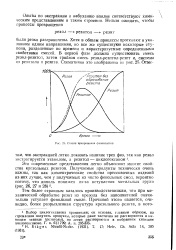 |
Стадии превращения фенопластов. [20] |
Опыты по экстракции и набуханию вполне соответствуют химическим представлениям о таком строении. [21]
Вместе с тем совершенно очевидно, что одних только химических представлений недостаточно для описания поведения органической фазы, которую в большинстве случаев ( при отсутствии в ней заметным образом диссоциированных веществ) можно рассматривать как смесь нескольких неэлектролитов, в том числе и образующихся в результате химического взаимодействия. Обратное утверждение было бы равносильно возвращению к теории Долежалека, отвергнутой ныне большинством физико-химиков и непригодной даже для качественного объяснения явления расслаивания. Между тем именно наличие двух несмешивающихся жидких фаз является характерной отличительной особенностью всех экстракционных систем. В качестве примера явлений, трудно объяснимых с чисто химических позиций, можно указать также на общеизвестные факты влияния природы химически инертного разбавителя на экстрагируемость данного элемента при неизменных прочих условиях. [22]
 |
Название соединений по имени их открывателей. [23] |
Экспериментальные наблюдения Тассзра не могли быть объяснены на основе химических представлений, существовавших в то время; необходимо было понять, как СоС1з и NHa, сами по себе устойчивые соединения, по-видимому с насыщенной валентностью, могут реагировать и давать другое очень устойчивое химическое соединение. [24]
Строение п свойства этих форм часто плохо укладываются в рамки привычных химических представлений. Гетерогенный катализ реакций газов и жидкостей твердыми телами до сих пор трудно поддается однозначной теоретической интерпретации. Усложнение кинетики и механизма реакций с участием твердых тел по сравнению с кинетикой и механизмом аналогичных гомогенных реакций вызвано в первую очередь наличием поверхностных явлений, в механизме которых фактор неопределенности гораздо выше, чем в объемных. Это связано с недостаточной изученностью природы химических связей в твердых телах, особенно на их поверхности. [25]
Характерная черта работ отечественных исследователей - глубокая связь между развитием общих химических представлений о природе химических соединений, понятием о химическом индивиде, о химическом сродстве, с одной стороны, и проблемой растворов, - с другой. Менделеева, и такая внутренняя связь в более или менее четкой форме всегда существовала и но многих работах последующего периода. [26]
Характерная черта работ отечественных исследователей - глубокая связь между развитием общих химических представлений о природе химических соединений, понятием о химическом индивиде, о химическом сродстве, с одной стороны, и проблемой растворов, - с другой. Менделеева, и такая внутренняя связь в более или менее четкой форме всегда существовала и но многих работах последующего периода. [27]
Обычно часть гипотез удается отбросить сразу же, исходя из общих химических представлений. В данном случае мы ограничимся подробным анализом правильности ( корректности) схем II и III, полагая их наиболее химически достоверными. [28]
Таким образом, для металлов I-VI групп естественное с точки зрения обычных химических представлений предположение о том, что при сближении их атомов в кристаллическом состоянии благодаря возбуждению их внешних оболочек происходит коллективизация всех внешних валентных электронов, приводит к заключению, что их ионы должны обладать внешними заполненными рв-оболочками. Обменное взаимодействие шести ортогонально направленных электронных облаков этой оболочки с шестью соседними ионами приводит к организации таких ионов в объем-ноцентрированную структуру, свойственную этим металлам в широком интервале температур или по крайней мере вблизи температуры плавления в качестве наиболее высокотемпературной модификации. [29]
Мы видим здесь, как на помощь устарелым представлениям о контакте приходят устарелые химические представления. Согласно новейшим воззрениям, соль есть кислота, в которой водород замещен каким-нибудь металлом. Рассматриваемый нами процесс подтверждает это воззрение: прямое вытеснение водорода кислоты цинком вполне объясняет происходящее здесь превращение энергии. Прежнее воззрение, которого придерживается Видеман, считает соль соединением какого-нибудь металлического окисла с какой-нибудь кислотой и поэтому говорит не о сернокислом цинке, а о сернокислой окиси цинка. Но для получения в нашей цепи из цинка и серной кислоты сернокислой окиси цинка необходимо, чтобы цинк сперва окислился. [30]
Страницы: 1 2 3 4