Легкое замещение
Cтраница 2
По Тарранту, реакционноспособность 1 1 1 3-тетрахлор - З - ме-тилбутана в последней реакции объясняется промежуточным образованием олефина СС1зСНС ( СН3) СН3, в котором аллиль-ные атомы хлора подвергаются легкому замещению. [16]
Кнунянц, Б. Л. Дяткнн и Н. П. Гамбарян [22], образование четырехчленного кольца происходит не потому, что оно предпочтительнее в энергетическом отношении перед другими циклическими системами, а потому, что атомы брома в исходном тетракарбоновом эфире становятся положительными и поэтому способными к легкому замещению на натрий. Кольцо же образуется в результате внутримолекулярной циклизации, которой способствует пространственное расположение двух углероднобромных групп эфира. [17]
Другим примером веществ с подвижной аминогруппой могут служить соединения, содержащие аминогруппу в аллильном положении. Способность таких веществ к легкому замещению аминогруппы была открыта в 1911 г. А. Е. Порай-Кошицем с сотрудниками. [18]
Так, на следующем этапе - через 2 - 2 5 месяца после травмы возможность непосредственного воспроизведения рассказов стала относительно доступной и от прежнего синдрома осталось лишь легкое замещение отдельных фрагментов рассказа побочными ассоциациями и явлениями, близкими к парамнезии, которые выступали только при передаче содержания относительна сложных рассказов. [19]
По мнению авторов, каталитическая активность может быть обеспечена металлами, имеющими высокий заряд и вакантные d - орбитали. Эти металлы не должны принимать участия в реакциях одноэлектронного окисления-восстановления. Комплексы металлов должны содержать лиганды, способные к легкому замещению в координационной сфере. [20]
Как было установлено, высокая каталитическая активность в этой реакции может быть обеспечена металлами, имеющими высокий заряд и вакантные а-орбитали. Кроме того, эти металлы не должны принимать участия в реакциях одноэлектронного окисления - восстановления. Комплексы этих металлов должны содержать лиганды, способные к легкому замещению в координационной сфере. Всем этим требованиям в наибольшей степени отвечают молибден и ванадий. [21]
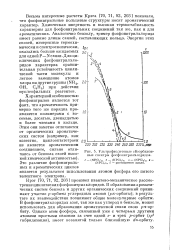 |
Ультрафиолетовые абсорбционные спектры фосфонитрилхлоридов. [22] |
Химическая инертность и высокая термостабильность характерны для фосфонитрильных соединений так же, как и для ароматических. Аналогично бензолу, тример фосфонитрилхлорида имеет равные длины связей, составляющих кольцо. Энергии этих связей, измеренные термохимически и спектроскопически, оказались больше ожидаемых для одной Р - N связи. Для циклических фосфонитрилхлоридов характерна сравнительная устойчивость циклической части молекулы и легкое замещение атомов хлора на другиегруппы ( NR2, ОН, С6Н5) при действии нуклеофильных реагентов. [23]
Иначе говоря, при таком развитии событий исключается процесс, который завершал бы механизм присоединения. Невозможно кратко рассмотреть обширную литературу, касающуюся относительных реакционных способностей и соотношений изомеров при нитровании в ароматическом ряду. Большинство этих работ предшествовало периоду, когда появились сколько-нибудь точные сведения о механизме протекающих реакций, и очень интересно поэтому рассмотреть общее значение нашей концепции. Довольно давно было уяснено, что отрицательные атомы углерода реакционноспособны в реакциях ароматического замещения. Позднее более современным способом описания этого эффекта явилось указание на то, что легкое замещение обусловливается избытком электронной плотности у реакционного центра. [24]
Иначе говоря, при таком развитии событий исключается процесс, который зяпепшал бы механизм присоединения. Невозможно кратко рассмотреть обширную литературу, касающуюся относительных реакционных способностей и соотношений изомеров при нитровании в ароматическом ряду. Большинство этих работ претшестно-вало периоду, когда появились сколько-нибудь точные сведения о механизме протекающих реакций, и очень интересно поэтому рассмотреть общее значение нашей концепции. Довольно давно было уяснено, что отрицательные атомы углерода реакционноспособны в реакциях ароматического замещения. Позднее более современным способом описания этого эффекта явилось указание на то, что легкое замещение обусловливается избытком электронной плотности у реакционного центра. [25]
Еще в 1864 году Беренд [1, 2] показал, что дииод-ацетилен может быть получен при встряхивании ацети-ленида серебра с эфирным раствором иода. Иоцич [4] получал дииодацетилен прямо при действии иода на димагний-бромацетилен. Было также обнаружено, что сам ацетилен реагирует с галоидами и их соединениями в щелочной среде и дает дига-лоидоацетилен. Возможно, что эта реакция протекает за счет небольших количеств иона ацетиленида, существующего в условиях равновесия в водных щелочных растворах. В этом случае также замещаются оба водородных атома, и, невидимому, замещение галоидом одного атома водорода ацетилена способствует более легкому замещению и второго атома водорода. [26]
Изучение свойств динитропродукта в нашей работе было ограничено нахождением условий восстановления изомерного ( 4, у) динитрофлуорантена с 7 пл 288 - 289 и попыткой замены в нем нитрогрупп на хлор. Полученный диамин имел Тил 164 - 165, выход 30 % - Анализ на азот ( по ( Кьельдалю) полученного диаминфлуорантена показал, что полностью восстанавливалась только одна нитрогруппа. Серия опытов, проведенных с целью замены нитрогрупп в динитрофлуорантене с помощью РС13 и SOCU при температурах 120 - 180, показала, что происходит не только легкое замещение нитрогрупп на хлор, но и одновременно дальнейшее вхождение в молекулу флуорантена третьего и даже четвертого атома хлора. Во всех опытах получалось, судя по анализам на хлор, смесь хлорпроизвод-1 ых флуорантена. [27]
Еще более сложно иротекае. Сколько-нибудь подробно описаны только бромнрование и иодирование нмидазола. Прямое хлорирование, по-видимому, дает неопределенные продукты, но в реакции с гипохлоритом натрия, N-хлорсукцинимидом, N-хлорфталимндом при тщательном соблюдении условий образуются 4 - и 5-хлорзамещенные соединения. Однако имидазол очень легко реагирует с бромом в хлороформе, воде и эфире с образованием 2 4 5-трибромпмидазола. Столь же трудно избежать бромировапия по всем свободным положениям и с 1-алкилимидазоламн. Особенность этих реакций - легкое замещение у С-2, чем они резко отличаются от нитрования. [28]
Еще более сложно протекает галогенирование; вариации реакции значительны и зависят от реагента, субстрата, реакционных условий. Сколько-нибудь подробно описаны только бронирование и иодирование имидазола. Прямое хлорирование, по-видимому, дает неопределенные продукты, но в реакции с гипохлоритом натрия, N-хлорсукцинимидом, N-хлорфталимидом при тщательном соблюдении условий образуются 4 - и 5-хлорзамещенные соединения. Однако имидазол очень легко реагирует с бромом в хлороформе, воде и эфире с образованием 2 4 5-трибромимидазола. Столь же трудно избежать бромирования по всем свободным положениям и с 1-алкилимидазолами. Особенность этих реакций - легкое замещение у С-2, чем они резко отличаются от нитрования. [29]
Страницы: 1 2