4-диол
Cтраница 2
Другие пути, включающие циклическое гидроборирование, показаны на схемах ( 292) и ( 293); последний пример иллюстрирует возможность достижения стерео-и региоселективного контроля. Созданы также конструкционные синтезы 1 3 - и 1 4-диолов с использованием борорганических реагентов. [16]
Общий метод синтеза фурана или его производных состоит в дегидратации алифатических 1 4-диолов или 1 4-дикетонов. [17]
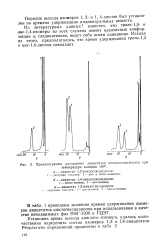 |
Хроматограмма разделения диацетатов циклогександиолов при температуре колонки 140. [18] |
Из литературных данных3 известно, что гране-1 3 - и цмс-1 4-изомеры во всех случаях имеют идентичные конфор-мации и, следовательно, ведут себя почти одинаково. Исходя из этого, предполагалось, что время удерживания т / гакс-1 3 и цис-1 4-диолов совпадает. [19]
У этих соединений наблюдаются интересные отличия в свойствах по сравнению с рассмотренными ранее членами ряда. В то время как у 1 2-диолов Av монотонно возрастает при уменьшении азимутального угла между ОН-группами, у 1 4-диолов это не происходит. Максимальное значение Av в случае 1 4-диолов достигается, по-видимому, при углах, равных 90, а при уменьшении или увеличении угла Av уменьшается. Кун объясняет этот результат с учетом разрешенных конформаций 1 4-диолов. [20]
Следует отметить крайнюю ограниченность литературных данных относительно восстановления такого типа соединений, в связи с чем авторам пришлось значительное время уделить методике выделения получающихся 1 4-диолов. Особые трудности встретились при получении низкомолекулярных, плохо растворявшихся в эфире и довольно хорошо растворимых в воде гликолей. [21]
В ряде случаев из 1 2-диолов, особенно из тетраарилзаме-щенных диолов, в условиях пинаколиновой перегруппировки образуются оксираны, однако эта реакция не является общим методом их получения. Как оксираны, так и оксетаны, получающиеся сходным образом из 1 3-диолов [474], легко подвергаются катализируемой кислотой перегруппировке или дальнейшей дегидратации. Напротив, циклизация 1 4-диолов служит главным путем получения тстрагпдрофуранов; 1 5-диолы сходным образом могут быть превращены в тетрагндропираны. [22]
В ряде случаев из 1 2-диолов, особенно из тетраарилзаме-щенных диолов, в условиях пинаколииовой перегруппировки образуются оксираны, однако эта реакция не является общим методом их получения. К ак оксираны, так и оксетаны, получающиеся сходным образом из 1 3-диолов [474], легко подвергаются катализируемой кислотой перегруппировке или дальнейшей дегидратации. Напротив, циклизация 1 4-диолов служит главным путем получения тетрагидрофуранов; 1 5-диолы сходным образом могут быть превращены в тетрагидропираны. [23]
У этих соединений наблюдаются интересные отличия в свойствах по сравнению с рассмотренными ранее членами ряда. В то время как у 1 2-диолов Av монотонно возрастает при уменьшении азимутального угла между ОН-группами, у 1 4-диолов это не происходит. Максимальное значение Av в случае 1 4-диолов достигается, по-видимому, при углах, равных 90, а при уменьшении или увеличении угла Av уменьшается. Кун объясняет этот результат с учетом разрешенных конформаций 1 4-диолов. [24]
Вопрос проявления гликолей все еще окончательно не решен. Чувствительность проявления этим реактивом для а-глико-лей в десять раз меньше, чем для Сахаров; для 1 3 - или 1 4-диолов она еще в два раза меньше. Исходя из этого, на бумагу следует наносить от 100 до 500 г отдельных гликолей. [25]
У этих соединений наблюдаются интересные отличия в свойствах по сравнению с рассмотренными ранее членами ряда. В то время как у 1 2-диолов Av монотонно возрастает при уменьшении азимутального угла между ОН-группами, у 1 4-диолов это не происходит. Максимальное значение Av в случае 1 4-диолов достигается, по-видимому, при углах, равных 90, а при уменьшении или увеличении угла Av уменьшается. Кун объясняет этот результат с учетом разрешенных конформаций 1 4-диолов. [26]
Страницы: 1 2