Валентность - сера
Cтраница 3
Сера образует с фтором большее число соединений, чем с другими галогенами; только в соединениях с фтором проявляется характеристичная валентность серы. [31]
Докажите, что реакция ( 21) - окислительно-восстановительная и что одновременно с изменением валентности углерода при окислении изменяется и валентность серы. [32]
При реакции двувалентной серы с диолефинами, очевидно, можно ожидать не только структурирования; не исключена возможность, что обе валентности серы прореагируют с активными участками той же полимерной цепи, в результате чего произойдет замыкание цикла. [33]
Это явление можег быть объяснено энолизацией и образованием двойной связи между углеродом и серой или прямой ионизацией водорода. Вопрос о валентности серы возникает во всех случаях, когда сульфоно-вая группа активирует присоединенный водород и облегчает реакции галогенирования, конденсации или рацемизации. [34]
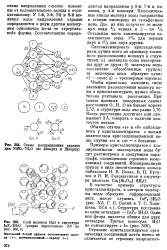 |
Схема распределения зарядов. для NiSCv7H20 ( по Биверсу и Шварцу.| Слой молекул Н20 в структуре ГпРз-ЗШО ( разрез параллельно АВ на 366 0. [35] |
Положительные концы молекул воды направлены к атомам кислорода из сульфатного иона. Остальная часть компенсируется валентностью серы: 13 / 5 для первых двух и 12Д для двух других. [36]
Напомним, что соединения, в которых валентность азота равна 4, содержат одну координационную связь. Подобным образом соединения серы, в которых валентность серы больше 2, имеют одну или две координационные связи. [37]
В табл. 21 - 1 приведен ряд типичных соединений, содержащих серу, а также их тривиальные названия и названия по системе IUPAC. Часто оказывается удобным классифицировать сернистые производные в соответствии с валентностью серы в этих соединениях. Из данных табл. 21 - 1 следует, что производные двухвалентной серы в структурном отношении сходны с соединениями кислорода, типы которых были рассмотрены в предыдущих главах. [38]
В табл. 21 - 1 приведен ряд типичных соединений, содержащих серу, а также их тривиальные названия и названия по системе ШРАС. Часто оказывается удобным классифицировать сернистые производные в соответствии с валентностью серы в этих соединениях. Из данных табл. 21 - 1 следует, что производные двухвалентной серы в структурном отношении сходны с соединениями кислорода, типы которых были рассмотрены в предыдущих главах. Такие производные серы часто называют, используя частицу тио и название соответствующего кислородного аналога. [39]
Сернистый газ химически весьма активен. Характерные для него реакции можно разбить на три группы: а) протекающие без изменения валентности серы, б) связанные с ее понижением и в) идущие с ее повышением. [40]
Двуокись серы химически весьма активна. Характерные для нее реакции можно разбить на три группы: а) протекающие без изменения валентности серы, б) связанные с ее понижением и в) идущие с ее повышением. [41]
Диоксид серы химически весьма активен. Характерные для него реакции можно разбить на три группы: а) протекающие без изменения валентности серы, б) связанные с ее понижением и в) идущие с ее повышением. [42]
Свободная электронная пара в соединениях, содержащих трехвалентную серу ( как ц в случае фосфинов), не обладает такой подвижностью, как в соединениях азота, и потому удалось синтезировать оптически активные сульфониевые соли, сульф-оксиды, эфиры сульфиновой кислоты и сульфиниламины. Конфигурационная устойчивость этих трехвалентных асимметрических атомов по сравнению с атомами азота, вероятно, обусловлена тем, что благодаря большим межатомным расстояниям пирамида, образованная валентностями серы или фосфора, несколько выше, чем пирамида, образованная валентностями азота. [43]
Страницы: 1 2 3