Освободившаяся валентность
Cтраница 2
Если положительный элемент с данной валентностью и данным координационным числом замещает другой положительный элемент, имеющий более высокую валентность, но такое же координационное число, то полученное вещество только в том случае будет иметь свойства катализатора, если освободившиеся валентности будут насыщены с помощью водородных ионов. [16]
Как видно из уравнения, от бензольного ядра отщепляется один атом водорода, а от молекулы серной кислоты-водный остаток. Освободившиеся валентности атомов углерода и серы взаимно насыщают друг друга. В результате реакции получается бензолсульфокислота, в которой атом углерода бензольного кольца соединен с атомом серы. [17]
Как видно из уравнения, от бензольного ядра отщепляется один атом водорода, а от молекулы серной кислоты - водный остаток. Освободившиеся валентности атомов углерода и серы взаимно насыщают друг друга. В результате реакции получается бензолсульфокислота, в которой атом углерода бензольного кольца соединен с атомом серы. [18]
В некоторых случаях, когда условия особо жестки, тихий электрический разряд расщепляет в молекулах связь С - С. Однако обычно наблюдается дегидрогенизация, за которой следует полимеризация по освободившимся валентностям. В этом отношении действие тихого разряда походит на действие высоких температур, как это показал Davis 58 на примере ацетона и бензола. Разница между этими двумя видами действия электричества заключается в том, что при высокой температуре большая часть вещества превращается в продукты с более низким молекулярным весом, тогда как в тихом электрическом разряде получаются более высокие выхода продуктов конденсации и полимеризации. [19]
Кажется странным, что двойная связь не приводит к упрочению структуры, а, наоборот, является ахиллесовой пятой каждого соединения. Дело в том, что двойная связь легко разрывается, и к освободившимся валентностям присоединяются другие атомы или атомные группы. Это становится более понятным, если вспомнить, что дополнительная связь возникла только потому, что в момент образования молекулы не было никакой иной возможности насыщения валентностей углерода. [20]
С этой целью готовое изделие подвергают кратковременному радиоактивному облучению. Под влиянием его из отдельных звеньев макромолекул полиэтилена отрывается водород, и освободившимися валентностями углеродные атомы соседних макромолекул соединяются между собой, образуя структуру редкой сетки. [21]
Ненасыщенные углеводороды открытого строения - алкены ( общая химическая формула С Н2п) - имеют одну двойную связь между соседними атомами углерода. Они обладают способностью к реакциям присоединения, ибо двойная связь легко разрывается и за счет освободившейся валентности углерода происходит присоединение нового атома или атомной группы. Токсическое действие алкенов сходно с действием алканов. [22]
Ненасыщенные углеводороды открытого строения - алкены ( общая химическая формула СПН2П) - имеют одну двойную связь между соседними атомами углерода. Они обладают способностью к реакциям присоединения, ибо двойная связь легко разрывается и за счет освободившейся валентности углерода происходит присоединение нового атома или атомной группы. Токсическое действие алкенов сходно с действием алканов. Во избежание повышения упругости паров сжиженный газ не должен содержать значительных качеств этана, а для недопустимого снижения упругости - пентана. [23]
Под алкилированием подразумевается химическая реакция взаимодействия насыщенного парафинового либо ароматического углеводорода с олефинами. При алкили-ровании происходит перемещение атомов водорода от парафиновой либо ароматической углеводородной молекулы к олефину с присоединением последнего по месту освободившейся валентности. [24]
Этилен в отличие от предельных углеводородов обладает высокой химической активностью - способностью к реакциям присоединениям. Двойная связь в молекулах этилена при действии различных веществ легко разрывается, остается простая связь, и за счет освободившихся валентностей происходит присоединение новых атомов или атомных групп. [25]
Мы видим, что в нашей задаче свободный электрон решетки вновь выступает в роли свободной валентности. Эта свободная валентность, блуждающая по поверхности кристалла, вызывает разрыв валентной связи внутри молекулы АВ и насыщается за счет освободившейся валентности. [26]
 |
Физические свойства некоторых алкенов. [27] |
Химические свойства олефинов определяет двойная углерод-углеродная связь. При действии на двойную связь различных реагентов разрывается та связь, которая образована л-электронами ( л-связь), как наименее прочная и более реакционноспособная. В результате разрыва л-связи освободившиеся валентности углеродных атомов затем затрачиваются на присоединение атомов или групп атомов молекулы реагента. Присоединение к двойной углерод-углеродной связи в большинстве случаев носит электрофильный характер ( АЕ); при этом двойная связь, являясь донором электронов, проявляет нуклеофильные свойства. [28]
Химические свойства олефинов определяет двойная углерод - углеродная связь. При действии на двойную связь различных реагентов разрывается та связь, которая образована я-электронами ( я-связь) как наименее прочная и более реакционноспособная. В результате разрыва я-связи освободившиеся валентности углеродных атомов затем затрачиваются на присоединение атомов или групп атомов молекулы реагента. Присоединение к двойной углерод - углеродной связи в большинстве случаев носит электрофильный характер ( Лв); при этом двойная связь, являясь донором электронов, проявляет нуклеофильные свойства. [29]
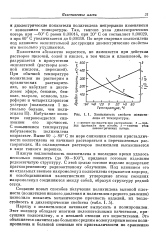 |
Зависимость свойств полиэтилена от температуры. [30] |
Страницы: 1 2 3