Главная валентность
Cтраница 2
Силы главной валентности во внутрикомплексных соединениях отмечают сплошной чертой, побочные-стрелкой, направленной к центральному атому комплексообразователя. [16]
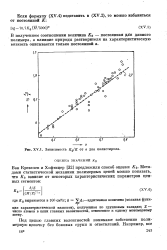 |
Зависимость KQ / K от а для полистирола. [17] |
Под цепью главных валентностей понимают собственно полимерную цепочку без боковых групп и ответвлений. [18]
 |
Строение цепей главных валентностей целлюлозы ( а и крахмала ( б ( атомы кислорода заштрихованы. [19] |
Цепочки главных валентностей крахмала сильно изогнуты, вследствие чего частицы его более рыхлы, чем у клетчатки, характеризующейся плотным скелетом. [20]
Цепь главных валентностей нуклеиновой кислоты образована попеременно эфирносвязанной фосфорной кислотой и сахаром, рибозой или дезоксирибозой, соединенной с фосфорной кислотой эфирной связью в 3 и 5 атомах углерода фуранозного цикла. [21]
Так как главные валентности атомов М и X внутри такого слоя насыщены, то между соседними слоями имеются только ван-дер-вааль-совские силы. Такой слой можно рассматривать как бесконечную двумерную молекулу; с химической точки зрения мы больше интересуемся внутренним строением такого слоя, чем способом упаковки последовательных слоев. Следует только напомнить, что такие сложные слои могут упаковываться друг с другом различными способами, приводя к кубической или гексагональной, или к какой-либо иной плотной упаковке атомов галоида во всей структуре. Поэтому можно ожидать, что существуют две структуры, связанные между собой таким образом и имеющие идентичные слои X - М - X. В плотной упаковке атомов число октаэдрических пустот равно числу плотно упакованных атомов; следовательно, если все пустоты заняты, то соединение имеет формулу MX. В структуре каменной соли ионы хлора находятся в плотной кубической упаковке, а ионы натрия - в октаэдрических пустотах между шестью ионами хлора. Однако в большинстве галоидных солей щелочных металлов ионы щелочных металлов слишком велики для октаэдрических пустот между плотно упакованными ионами галоида, и поэтому последние уже не соприкасаются друг с другом, а соприкасаются только с окружающими их шестью ионами щелочного металла. [22]
Из определения главных валентностей вытекает также, что эти силы действуют как между двумя атомами различных молекул, так и между двумя атомами одной молекулы. Силы главных валентностей, как можно легко себе представить, связывают молекулы мономеров в полимерную молекулу. Здесь следует помнить о функциональности, имея в виду, что полимер может образоваться только в том случае, если мономер имеет соответствующую функциональность. При взаимодействии этилового спирта с уксусной кислотой полимер не может образоваться, так как эти соединения монофункциональны. Однако силы главных валентностей проявляются при взаимодействии этих соединений. Силы главных валентностей действуют также в процессе полимеризации льняного масла, при получении гликольадипината, полистирола и других упомянутых выше соединений. [23]
Прочность цепей главных валентностей достаточно велика, хотя несомненно, что с увеличением длины цепи начинает проявляться склонность к термическому распаду. Стойкость к механическим воздействиям тоже относительно велика, однако действие ультразвуковых колебаний может быть причиной значительной деполимеризации. [24]
Цепь их главной валентности также построена из атомов металла и кислорода. [25]
Помимо сил главных валентностей, связывающих атомы главной цепи, существуют вторичные силы ( силы Ван-дер - Ваальса), действующие между макромолекулами. Кроме того, между макромолекулами хорошо ориентированных волокон возникают довольно сильные водородные связи. Наличие водородных связей в значительной степени определяет свойства волокон. Своим происхождением связи этого типа обязаны способности атома водорода проявлять валентность, большую единицы. [26]
Обрамляющие группы главных валентностей не попадают в поле механических напряжений и поэтому они непосредственно не активируются. [27]
Из определения главных валентностей вытекает также, что эти силы действуют как между двумя атомами различных молекул, так и между двумя атомами одной молекулы. Силы главных валентностей, как можно легко себе представить, связывают молекулы мономеров в полимерную молекулу. Здесь следует помнить о функциональности, имея в виду, что полимер может образоваться только в том случае, если мономер имеет соответствующую функциональность. При взаимодействии этилового спирта с уксусной кислотой полимер не может образоваться, так как эти соединения монофункциональны. Однако силы главных валентностей проявляются при взаимодействии этих соединений. Силы главных валентностей действуют также в процессе полимеризации льняного масла, при получении гликольадипината, полистирола и других упомянутых выше соединений. [28]
В этих случаях главная валентность центрального атома насыщается вне пределов комплексного иона за счет кислотных остатков, связанных со всем комплексом. Группы, не входящие в состав самого комплексного иона и лишь нейтрализующие его заряд, называют находящимися во внешней координационной сфере. [29]
В результате проявления главной валентности образуются молекулы соединений первого порядка, строение которых может быть вполне удовлетворительно истолковано обычным учением о валентности без каких-либо дополнительных гипотез. [30]
Страницы: 1 2 3 4