Максимальная положительная валентность
Cтраница 3
Из элементов подгруппы ванадий - ниобий-тантал наибольшее практическое значение имеет ванадий и его соединения. Максимальная положительная валентность этих элементов, равная 5, обусловливается потерей атомами этих элементов пяти валентных электронов. В атомах ванадия и тантала на внешнем слое находится 2 электрона, в слое, соседнем с внешним, ( 8 3) электронов, а в атоме ниобия, соответственно 1 и ( 8 4) электронов. [31]
Виснут находится в 5А подгруппе периодической системы элементов, в его внешнем квантовом слое электронной оболочки имеются 5 электронов. Максимальная положительная валентность висмута равна пяти; известны соединения, где висмут проявляет отрицательную валентность, равную трем. [32]
Максимальная положительная валентность элементов побочной подгруппы обусловливается способностью их атомов отдавать электроны как внешнего, так и второго снаружи энергетического уровня. [33]
Она определяется, как правило, группой периодической системы Д. И. Менделеева, в которй находится данный элемент. Максимальная положительная валентность элементов главных подгрупп периодической системы равна номеру группы. Валентность элементов в соединении условно определяется числом электронов, потерянных или приобретенных атомами, образовавшими данную молекулу. [34]
Она определяется, как правило, группой периодической системы Д. И. Менделеева, в которой находится данный элемент. Максимальная положительная валентность элементов главных подгрупп периодической системы равна номеру группы. Валентность элементов в соединении условно определяется числом электронов, потерянных или приобретенных атомами, образовавшими данную молекулу. Валентность многих элементов изменяется в зависимости от условий протекающего процесса. Водород всегда одновалентен, кислород - двухвалентен. [35]
Структура внешнего слоя атомов серы, селена и его аналогов обусловливает их преимущественно металлоидный характер с максимальной отрицательной валентностью, равной двум. Максимальную положительную валентность серы, селена и его аналогов можно ожидать равной шести, причем электроны должны отдаваться ими легче, чем стоящими в том же горизонтальном ряду галоидами. [36]
Структура внешнего слоя атомов серы, селена и его аналогов обусловливает их преимущественно металлоидный характер с максимальной отрицательной валентностью, равной двум. Максимальную положительную валентность серы, селена и его аналогов можно ожидать равной шести, причем электроны должны отдаваться ими легче, чем стоящими в том же горизонтальном ряду галогенами. [37]
Наличие во внешнем слое атомов лишь одного или двух электронов обусловливает металлический характер элементов подгруппы хрома. Вместе с тем их максимальная положительная валентность также должна быть равна шести. [38]
Наличие во внешнем слое атомов лишь одного или двух электронов обусловливает мета л-л и чески и характер элементов подгруппы хрома. Вместе с тем их максимальная положительная валентность также должна быть равна шести. [39]
Наличие во внешнем слое атомов лишь одного или двух электронов обусловливает металлический характер элементов подгруппы хрома. Вместе с тем их максимальная положительная валентность также должна быть равна шести. [40]
Таким образом, валентное число инертных газов равно нулю. Чтобы согласовать номер группы инертных газов с максимальной положительной валентностью, как это сделано для остальных групп периодической системы, эта группа была названа нулевой группой и помещена в начале периодической системы. При непрерывном расположении элементов, принятом в табл. II ( см. приложение), инертные газы попадают в восьмую группу в качестве ее главной подгруппы. Такое расположение согласуется с закономерностями периодической системы, так как при уменьшении отрицательной валентности с возрастанием номера группы, начиная с четвертой главной подгруппы, нулевую валентнооть следует ожидать для элементов восьмой главной подгруппы. Двойственность положения инертных газов соответствует их особому характеру по сравнению с элементами остальных главных подгрупп. Подробнее об этом будет сказано в следующей главе. [41]
Таким образом, валентное число инертных газов равно нулю. Чтобы согласовать номер группы инертных газов с максимальной положительной валентностью, как это сделано для остальных групп периодической системы, эта группа была названа нулевой группой и помещена в начале периодической системы. При непрерывном расположении элементов, принятом в табл. II ( см. приложение), инертные газы попадают в восьмую группу в качестве ее главной подгруппы. Такое расположение согласуется с закономерностями периодической системы, так как при уменьшении отрицательной валентности с возрастанием номера группы начиная с четвертой главной подгруппы - нулевую валентность следует ожидать для элементов восьмой главной подгруппы. Двойственность положения инертных газов соответствует их особому характеру по сравнению с элементами остальных главных подгрупп. Подробнее об этом будет сказано в следующей главе. [42]
Таким образом, валентное число инертных газов равно нулю. Чтобы согласовать номер группы инертных газов с максимальной положительной валентностью, как это сделано для остальных групп периодической системы, эта группа была названа нулевой группой и помещена в начале периодической системы. При непрерывном расположении элементов, принятом в табл. II ( см. приложение), инертные газы попадают в восьмую группу в качестве ее главной подгруппы. Такое расположение согласуется с закономерностями периодической системы, так как при уменьшении отрицательной валентности с возрастанием номера группы, начиная с четвертой главно. Двойственность положения инертных газов соответствует их особому характеру по сравнению с элементами остальных главных подгрупп. Подробнее об этом будет сказано в следующей главе. [43]
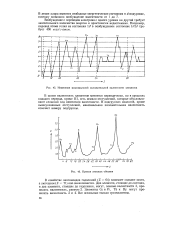 |
Изменение максимальной положительной валентности элементов.| Кривая атомных объемов. [44] |
В целом валентность элементов меняется периодически, но в пределах каждого периода, кроме III, есть немало отступлений, которые обусловливают сложный ход изменения валентности. В подгруппах аналогов, кроме вышеуказанных отступлений, максимальная положительная валентность отвечает номеру подгруппы. [45]
Страницы: 1 2 3 4