Природа - ионит
Cтраница 1
Природа ионита также влияет на стабильность. [1]
В зависимости от природы ионитов и обменивающихся ионов, а также от их концентрации время установления ионообменного равновесии колеблется от нескольких минут до нескольких суток. [2]
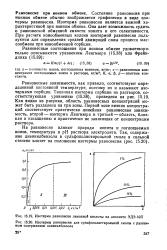 |
Изотерма равновесия лимонной кислоты на анионите ЭДЭ-10П.| Изотермы равновесия для сульфополистирольной смолы с различным содержанием дивинилбензола. [3] |
На равновесие влияют природа ионита и поглощаемых ионов, температура и рН раствора электролита. [4]
В понятие о природе ионита входит химическое строение матрицы, содержание сшивающего агента, являющееся мерой степени сшивки ( поперечной связанности), степень ( или константа) электролитической диссоциации активных групп, характер противоионов. [5]
Из такого представления о природе ионитов логически вытекает необходимость признания подвижной ионной атмосферы у поверхности твердой фазы ионита, образующейся в результате его диссоциации в присутствии растворителя. [6]
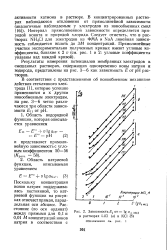 |
Зависимость EJ от - lg a в растворах LiCl ( a и КС1 ( б Обозначения 1. [7] |
Интервал прямолинейной зависимости определяется природой ионита и природой хлорида. Следует отметить, что в растворах МН4С1 для электродов из ФМА и NaA линейная зависимость соблюдается вплоть до ЗМ концентраций. [8]
Степень регенерации зависит от емкости и природы ионита, природы удаляемых ионов ( выражающейся через значение константы обмена), количества ионита и других факторов. В частности, расход реагента на регенерацию возрастает с увеличением значения константы обмена вытесняемых ионов. Отсюда можно сделать вывод о целесообразности использования слабодиссоциированных ионитов, на которых значения констант обмена исследуемых ионов весьма малы. Возможности использования слабодиссоциированных ионитов будут рассмотрены на примере слабокислотных ка-тионитов. [9]
Эти ряды изменяются в зависимости от природы ионита, хромато-графируемых веществ, растворов, применяемых при элюировании, и внешних условий эксперимента. [10]
Степень диссоциации ионогенных групп, зависящая от природы ионита и свойств раствора, определяет кислотные и основные свойства иенита. [11]
За последние 30 лет наши представления о природе ионитов сильно изменились. [12]
Селективность электродов с такими мембранами зависит в основном от природы ионита, а не растворителя. [13]
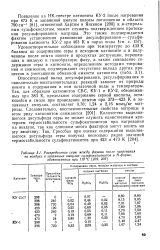 |
Распределение серы между фазами после нагревания. [14] |
Относительный вклад десульфирования, ресульфирования и окислительно-восстановительных реакций зависит от природы ионита и содержания в нем остаточной воды и температуры. Так, для образцов катионитов СБС, КУ-1 и КУ-2, обезвоженных при 383 К, предельное содержание серной кислоты, остающейся в смоле при проведении опытов при 373 - 423 К в запаянных ампулах, составляет 0 70; 1 24 и 2 16 моль / кг матрицы. Количество выделившегося дисульфида серы не может служить единственным критерием термостабильности сульфокатионитов при нагревании на воздухе, так как слишком много факторов могут влиять на эту величину. [15]
Страницы: 1 2 3 4