Природа - ионит
Cтраница 3
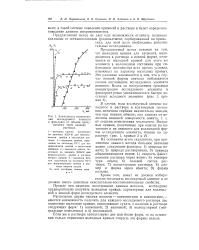 |
Зависимость концентрации исследуемого элемента в фильтрате от объема пропущенного через колонку раствора. [31] |
На основании всего сказанного, при применении данного метода большое значение имеют следующие факторы: 1) природа ионита; 2) природа растворителя; 3) природа обменивающихся ионов; 4) скорость фильтрования раствора через ионит; 5) температура опыта; 6) солевой состав раствора; 7) концентрация раствора; 8) размер и форма зерен ионита; 9) форма колонки. [32]
Здесь К и А - нерастворимые части ионита ( матрица, каркас), несущие заряд, который определяет природу ионита: отрицательный - у катионитов и положительный - у анионитов. [33]
Рациональный выбор температуры, продолжительности экспозиции, мощности излучения и концентрации растворов при любом воздействии этих факторов должен определяться природой ионита и его ионной формой. Во всех случаях это воздействие должно приводить к заметным изменениям ( до 10 - 20 %) свойств ионита. Проведение таких исследований при трех-четырех температурах с использованием уравнения Аррениуса позволит оценивать стойкость ионитов при любой температуре, обычно применяемой на практике. [34]
В соответствии с уменьшением радиусов гидратирован-ных ионов коэффициенты распределения увеличиваются в ряду Rb Cs Fr независимо от концентрации НС1 и природы ионита. [35]
Осмотическая составляющая обусловлена разностью парциальных давлений раствора в ионите и вне его, которые, в свою очередь, зависят от природы ионита ( сшитости, природы функциональных групп и матрицы), от концентрации раствора, природы растворенного вещества ( в частности, его ионного радиуса), температуры и давления. [36]
Все это определяет целесообразность рассмотрения на первой стадии описания равновесных свойств ионитов самых общих соотношений, характеризующих ионообменный процесс, безотносительно к природе ионита и специфики реализующихся в нем взаимодействий. Такие соотношения могут быть получены методами термодинамики. [37]
Величина Ка не зависит от концентрации микрокомпонента, но изменяется от природы второго обменивающегося вещества, состава раствора, температуры, давления и природы ионита. [38]
Коэффициенты распределения ионов не зависят от концентрации микрокомпонента, но изменяются в зависимости от природы второго обменивающегося иона, состава раствора, температуры раствора и природы ионитов. [39]
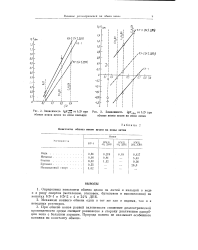 |
Зависимость lgK. от ID при [ IMAGE ] Зависимость lg - o6M от 1 / D при обмене ионов цезия па ионы кальция обмене ионов цезия на ионы лития. [40] |
При обмене ионов разной валентности снижение диэлектрической проницаемости среды смещает равновесие в сторону увеличения адсорбции иона с большим зарядом. Природа ионита не оказывает особенного влияния на константу обмена. [41]
При обмене ионов одной валентности снижение диэлектрической проницаемости растворителя смещает равновесие в сторону увеличения адсорбции иона с меньшим кристаллографическим радиусом и большей склонностью к ассоциации. Природа ионита и количество ДВБ в нем сильно сказываются на положении равновесия. [42]
Часто проявляется природа ионита. [43]
Для всех типов ионитов координационно-активными являются депротонированные ионогенные группы. В зависимости от природы ионита координационно-активная группа находится или в анионной ( катиониты) или в нейтральной ( аниониты) форме. [44]
Она зависит от природы ионита, свойств и концентрации обменивающихся ионов, а также в значительной степени от рН среды. [45]
Страницы: 1 2 3 4