Природа - комплекс
Cтраница 1
Природа комплекса, находящегося в равновесии с осадком, была изучена путем титрований исходных растворов растворами фосфатов. Установлено, что рН растворов фосфата алюминия, титруемых растворами однозамещенного фосфата, уменьшается с ростом концентрации фосфата. Это подтвердило, что образуется алюмофосфатный комплекс. Если бы такой комплекс не образовывался, то значение рН возрастало бы, так как в изученных пределах значений рН ион однозамещенного фосфата является основанием и присоединяет ионы водорода. Алюмофосфатный комплекс должен иметь основной характер, так как при добавлении щелочи к реакционной системе концентрация гидроксил-ионов увеличивается. Увеличение концентрации ОН - - ионов, соответствующее снижению рН в алюмофосфатной системе, может быть объяснено только образованием основного комплекса, который содержит связанные гидроксил-ионы. [1]
Природа комплекса активированная СО2 - хлорофилл, обозначенного в реакции (6.8) символом Хл. Активация углекислоты, по-видимому, тесно связана с карбокси-лированием у-аминомасляной кислоты, в результате которого образуется глутаминовая кислота. В последующей темновой реакции (6.9) 2 / 3 кислорода, выделившегося при световой реакции (6.8), и 2 / 3 одновременно ассимилированного углерода вновь образуют углекислоту. [2]
Природа комплексов, образованных при набухании, различна. Некоторые из них являются чисто адсорбционными комплексами и могут быть легко разрушены, но в некоторых случаях могут происходить реакции замещения с образованием эфиров и других производных целлюлозы. Поэтому каждое соединение следует исследовать отдельно. [3]
Природа мономер-катализаторного комплекса не известна, но вероятно, надо предполагать поляризацию молекулы. С другой стороны, заметное действие диэлектрической постоянной растворителя на полимеризацию такого тина заставляет предполагать, что в данном случае какую-то роль играют ионы. Таким образом, возможный инициирующим механизм хлорного олова с растворителем 80С14 С2Н4С13 - SnC17 C2H4Cl сопровождается комбинацией одного или другого иона с мономором. Подобные реакции известны с хлористым алюминием, и имеется доказательство наличия ионизационных процессов. Например, растворы хлорного олова в нитропарафинах обладают большой проводимостью. [4]
Относительно природы медно-целлюлозного комплекса высказывались различные мнения. Траубе [ 1571 считает, что одна часть меди связана с катионом, а другая - с анионом. Джолли 158 предположил, что отношение меди к целлюлозе 1: 1, так же как и в формуле Траубе, но вся медь связана с катионом. Гесс и Месмер [159] считают, что это соединение представляет собой комплексную соль. Позднее Ривз ( 160 - 163 ] сообщил данные, убедительно доказывающие, что медь связана с 2 - и 3-гидроксильными группами н, кроме того, что реакция целлюлозы с комплексами типа медноаммиачных может иметь место лишь в том случае, если обе эти гндроксильные группы являются свободными в одном и том же ангидроглюкозном остатке. Таким образом, медноаммиачная целлюлоза обладает структурой, представленной на стр. [5]
Сведения о природе комплексов серебра с роданином и его замещенными противоречивы. Файгль [237] установил, что эти реагенты взаимодействуют с металлами в 2-тион - 4-оксоформе, а не в таутомерных формах с гидро-ксильными или сульфгидрильными группами. [6]
Прямые доказательства относительно природы комплекса ( С02) скудны. Фиксация радиоактивной двуокиси углерода в темноте наблюдалась Рубеном, Хассидом и Каменом [99] у листьев ячменя и Рубеном, Каменом, Хассидом и Дево [100] у Chlorella. Они пользуются термином восстановление двуокиси углерода, которого мы предпочитаем избегать ( см. стр. [7]
Один из встречающихся в природе комплексов таких соединений - порфириновый комплекс Mg2 - описан несколько ранее. [8]
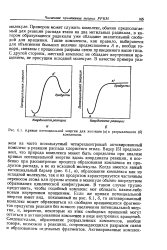 |
Кривые потенциальной энергии для жесткого ( а и разрыхленного. [9] |
Видер [5] предположил, что природа комплекса может быть определена при анализе кривых потенциальной энергии вдоль координаты реакции, и особенно при рассмотрении процесса образования комплекса из продуктов распада, а не из исходной молекулы. Когда имеется явный потенциальный барьер ( рис. 6.1, а), образование комплекса как из исходной молекулы, так и из продуктов характеризуется частичным переносом атома или группы атомов в молекуле обычно посредством образования циклической конфигурации. В таком случае трудно представить, чтобы подобный комплекс мог обладать каким-либо новым внутренним вращением. Если же кривая потенциальной энергии имеет вид, показанный на рис. 6.1, б, то активированный комплекс может образоваться из свободно вращающихся фрагментов продуктов реакции без всякого увеличения потенциальной энергии, и, вероятно, некоторые из этих свободных вращений могут остаться в активированном комплексе в виде внутренних вращений. Следовательно, образование разрыхленных комплексов, вообще говоря, возможно в реакциях, сопровождающихся разрывом связи и образованием отдельных фрагментов. [10]
В предыдущем разделе рассмотрено влияние природы комплекса на скорости кислотного гидролиза. [11]
Среди большого и разнообразного по своей природе комплекса методов, применяемых в химии и геохимии нефти, исключительно важное место занимают методы разделения ее компонентов. К ним прежде всего относятся различные виды перегонок: при атмосферном давлении и в вакууме, азеотропная, молекулярная и др. Не менее важное значение имеют методы хроматографическо-го разделения углеводородных и неуглеводородных компонентов нефти, включающие в себя вытеснительную, элюентную, тонкослойную, бу. [12]
Здесь А - постоянная, зависящая от природы комплекса. [13]
Выше в данной главе отмечалось, что природа комплексов, образующихся в реакциях ацетиленов с карбонилами железа, в значительной-степени зависит от условий проведения реакций. [14]
Как это чудесно, когда тебе открывается единая природа комплекса явлений, которые при непосредственном чувственном восприятии кажутся совершенно независимыми друг от друга. [15]
Страницы: 1 2 3 4