Природа - щелочной металл
Cтраница 4
Другой вопрос, требующий уточнения в связи L - представлением о равновесии ( 18), касается истинной природы свободных ионов. Как следует из абсолютных значений величин k, и k p, известных для стирола и некоторых других мономеров ( они различаются на 2 - 3 порядка), процессы полимеризации в соответствующих системах часто могут рассматриваться как протекающие практически полностью на свободных ионах. Это должно было бы иметь своим следствием независимость микроструктуры полимера от природы щелочного металла в системах типа ТГФ - металл - нафталин. Отсутствие сведений об абсолютных константах роста & р и / гр не позволяет подтвердить этот вывод кинетическими соображениями. Весьма вероятно, что свободные ионы в рассматриваемых анионных системах представляют собой образования, отличающиеся от карбанионов более сложным составом. По Виттигу, одним из возможных состояний металлоорганических соединении в растворе являются структуры типа [ R2Me ] - MeH. Конечно, для таких свободных анионов естественно сохранение индивидуальных особенностей, обусловленных природой входящего в их состав металла. [46]
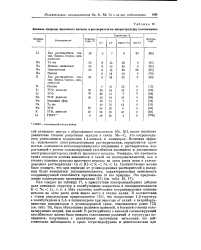 |
Влияние природы щелочного металла и растворителя на микроструктуру полиизопрена. [47] |
С, что сопровождается уменьшением содержания 1 4-звеньев в полимерах. Величина эффекта, вызываемого электронодонорными растворителями, определяется прочностью комплексов металлоорганического соединения с растворителем, возрастающей с ростом сольватирующей способности последнего и увеличением электроноакцепторных свойств щелочного металла. Очевидно, что прочность таких сольватов должна изменяться в такой же последовательности, как и степень влияния природы щелочного металла на акты роста цепи в углеводородных растворителях: Cs Rb; К Na Li. [48]
Обнаружено, что за исключением щелочных карбокси-латов, термоустойчивость других солей карбоновых кислот изменяется в одной и той же последовательности: серебряные медные кадмиевые цинковые бариевые и кальциевые. У щелочных солей алифатических монокарбоновых кислот устойчивость к тепловому воздействию повышается в ряду литий натрий калий. У бензоатов она в той же последовательности понижается. У оксалатов, орто -, изо - и терефталатов способность к распаду с выделением летучих продуктов практически не зависит от природы щелочного металла. [49]
Обнаружено, что за исключением щелочных карбокси-латов, термоустойчивость других солей карбоновых кислот, изменяется в одной и той же последовательности: серебряные медные кадмиевые цинковые бариевые и кальциевые. У щелочных солей алифатических монокарбоновых кислот устойчивость к тепловому воздействию повышается в ряду литий натрий калий. У бензоатов она в той же последовательности понижается. У оксалатов, орто -, изо - и терефталатов способность к распаду с выделением летучих продуктов практически не зависит от природы щелочного металла. [50]
В оптическом спектре метилтетрагидрофуранового раствора этого соединения при комнатной температуре имеются две полосы поглощения при 4550 и 5200 А, относительные интенсивности которых зависят от концентрации раствора. Быстрое охлаждение раствора до 77Э К приводит к образованию стекла, оптические свойства которого такие же, как и раствора. Спектр ЭПР состоит из резкой линии с g 2, обусловленной мономерными радикалами, и линий от переходов А / ия 1 и A / ns 2, характерных для три-плетного состояния. Относительные интенсивности синглетного и триплетного спектров ЭПР соответствуют относительным интен-сивностям полос оптического поглощения. Определен параметр D расщепления в нулевом поле, небольшая величина которого зависит от природы щелочного металла и составляет 333, 274 и 204 Мгц для ионов лития, натрия и калия соответственно. [51]
Относительно величины электромерного эффекта нельзя сказать ничего определенного, а при реакциях проявляет себя лишь карбениатное расположение. Растворимость в бензоле также, по-видимому, говорит о том, что в этом случае щелочной металл находится в ионном отношении преимущественно с карбениатной, а не с енольной формой. Имеется ли, кроме этого, еще и определенная доля гомеополярной связи углерод - щелочной металл, сказать в настоящее время нельзя. Этот вопрос затрагивает общую проблему состояния связи в соединениях углерода со щелочными металлами. Какой тип связи преобладает - гомеополярный, ионный или комплексный, - зависит в данном случае от природы щелочного металла, строения органического остатка, растворителя и даже от концентрации. В настоящее время идет интенсивное изучение этих взаимоотношений, поэтому более детальное обсуждение пока еще преждевременно. Для направления реакций типично мезомерных анионов это имеет меньшее значение. [52]
Страницы: 1 2 3 4