Природа - окислитель
Cтраница 2
Характер окисления целлюлозы зависит от рН среды и природы окислителя. В кислой и нейтральной средах образуются, как правило, оксицеллюлозы с преобладающим содержанием карбонильных групп. Эти препараты, имеющие свойства слабого восстановителя, называются оксицеллюлозами восстановительного типа. Для них характерны повышенны медные и йодные числа. При окислении в щелочной среде получаются окисленные целлюлозы, содержащие большое число карбоксильных групп. Такие целлюлозы обладают кислотными свойствами и называются оксицеллюлозами кислотного типа. [16]
Одни и те же органические соединения в зависимости от природы окислителя могут превращаться в различные соединения. Так, например, при окислении анилина хлорноватистой кислотой получают л-аминофенол, хромовой кислотой - л-хинон, надкисло тами - нитробензол. Различные продукты окисления могут образоваться не только при замене одного окислителя другим, но и в результате изменений условий, в которых действует один и тот же окислитель. Если, например, окислять анилин перманганатом калия в кислой среде, то происходит окислительная поликонденсация, приводящая к образованию анилинового черного. Если же окисление анилина перманганатом калия проводить в нейтральной среде, то продуктом реакции является азобензол, а в щелочной среде - нитробензол. [17]
Возможно также, что в зависимости от условий опыта и природы окислителя превращение спирта в альдегид может протекать или как собственно окисление ( гидроксилирование) согласно прежнему представлению, или же как дегидрирование. [18]
При окислении окиси этилена в зависимости от условий реакции и природы окислителя получаются либо гликолевая кислота, либо ( при глубоком окислении) двуокись углерода и вода. [19]
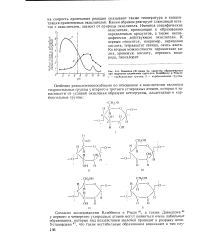 |
Влияние рН среды на характер образующихся при гидролизе целлюлозы групп ( по Клиббенсу и Ридге. [20] |
Каким образом реагирует глкжозный остаток с окислителем, зависит от природы окислителя. [21]
Возможно также, что в зависимости от условий опыта и природы окислителя превращение спирта в альдегид может протекать или как собственно окисление ( гидроксилированпе) согласно прежнему представлению, пли же как дегидрирование. [22]
Выход окисленного продукта зависит от длительности и температуры реакции и от природы окислителя. Окисление концентрированной ( 70 % - ной) азотной кислотой ( в течение 5 час при 100 С) приводит к образованию двух продуктов [6]: щелочерастворимого ( 65 %), получаемого при неглубоком окислении, и водорастворимого ( 30 %) - три глубоком окислении. Авторы [6] указывают, что окисление нафтеновых и ароматических составляющих приводит к появлению карбоксильных, карбонильных и гидроксильных групп. Пяти - и даже восьмикратное увеличение отношения N / C в окисленных продуктах по отношению к исходным обусловлено значительным нитрованием ароматического ядра. Почти неизменное соотношение S / H во всех продуктах окисления указывает на то, что сера содержится в гетероциклических фрагментах молекул, обладающих значительной устойчивостью. [23]
Направление окисления тетрагидро - ДП в очень сильной степени зависит от природы окислителя и растворителя. Так, иод в бензоле окисляет его до 4 4 - ДП, а в уксусной кислоте - до пиридина. Кислород воздуха окисляет до 4 4 - ДП, а тетраацетат свинца - до пиридина. [24]
Соединения марганца низших степеней окисления окисляются также в зависимости от среды и природы окислителя. [25]
 |
Кривые потенцио-метрического титрования железа ( П церием ( 1У в различных средах. [26] |
При титровании Fe11 до наступления конечной точки форма кривой не зависит от природы окислителя. [27]
Соединения марганца низших степеней окисления окисляются также в зависимости от среды и природы окислителя. [28]
Можно было предположить, что изменения в направлении окисления сульфита вызываются изменением природы окислителя. В щелочной среде процесс окисления сульфита замедляется в 1 4 раза, но относительный выход сульфата возрастает. [29]
Окисление анилина является очень сложным процессом, в ходе которого в зависимости от природы окислителя возможно образование фенилгидроксиламина, нитрозобензола, нитробензола, азобензола, азоксибензола, п-бензохинона или анилинового черного. [30]
Страницы: 1 2 3 4