Природа - водородная связь
Cтраница 1
 |
Значения ДЯ для водородных связей различных типов. [1] |
Природа водородной связи специфична. Атом Н не обобществляется полностью атомами А и В. Рентгенография не позволяет непосредственно определить положение атома водорода ( см. стр. Выяснилось, что обозначение О - Н - - - О реально обосновано - химическая связь О - Н существенно короче и, значит, прочнее водородной связи Н - - - О. При повышении температуры связи О - Н и Н - - - О могут меняться местами. Из квантовомеханиче-ского расчета, а также из общих соображений следует, что кривая зависимости энергии от положения атома Н в димере муравьиной кислоты имеет два симметричных минимума, разделенных активационным барьером. [2]
Природа водородной связи окончательно не выяснена. [3]
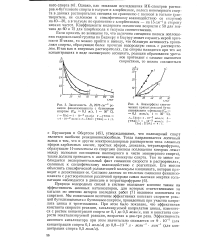 |
Зависимость Dt 2270 см-1 реакции фенилизоциаиата с бутиловым спиртом ( С 0 1 м / л, t 50 С.| Анаморфозы кинетических кривых реакций бути-лизоцианата с фенолом ( См 0 1 моль / л, t 50 С. [4] |
Природа водородных связей в системе оказывает влияние также на эффективность аминных катализаторов, для которых ответственными за катализ по мнению авторов последних работ [7] являются комплексы со спиртами. [5]
Природа водородной связи до конца не выяснена. [6]
Природа водородной связи не вполне еще выяснена. [7]
Природа водородной связи полностью не выяснена. [8]
Природа водородной связи до конца не выяснена. [9]
Природа водородной связи еще не вполне ясна. Можно сказать, что главную роль здесь играют следующие факторы. [10]
Природа водородной связи полностью не изучена. По-видимому, она имеет электростатический характер. Ковалентная связь между кислородом и водородом в группах О - Н поляризована, и осуществляющая ее электронная пара смещена к кислороду ( стр. Водород несет некоторый положительный заряд, кислород - отрицательный. Наличие этих зарядов и обусловливает притяжение атома водорода одной молекулы и атома кислорода другой. [11]
Природа водородной связи полностью не выяснена. То обстоятельство, что водород дает ее с электроотрицательными атомами, делает вероятным существенную роль электростатического взаимодействия. Маленький, положительно заряженный ион водорода способен дать значительную энергию связи с соседними отрицательными ионами. [12]
Относительно природы водородной связи высказывалось много соображений; опубликовано также несколько расчетов по методу ВС, но все это позволяет нарисовать лишь некоторую качественную картину. [13]
Уяснение природы водородной связи базируется на квантово-механических расчетах, и в последнее десятилетие здесь наблюдается существенное продвижение вперед как в отношении точности расчетов, так и по сложности исследуемых объектов. [14]
При рассмотрении природы водородной связи и ее влияния на различные свойства соединений следует различать системы без сопряженных л-связей и с л-сопряжением. [15]
Страницы: 1 2 3 4