Природа - агрессивная среда
Cтраница 1
Природа агрессивной среды и протекающие при ее контакте с металлами реакции определяют характер процесса коррозии металлов: электрохимический - в электролитах и химический - в сухих газах при высоких температурах или в жидких неэлектролитах. [1]
Природа агрессивной среды, ее агрегатное состояние, химический состав, размеры и конфигурация молекул в значительной степени влияют на интенсивность еорбционно-диффузионных процессов в полимерах. Сорбция органических жидкостей и их паров в полимерах определяется размерами и конфигурацией ее молекул. [2]
Природа агрессивной среды и протекающие при ее контакте с металлами реакции определяют характер процесса коррозии металлов: электрохимический - в электролитах и химический - в сухих газах при высоких температурах или в жидких неэлектролитах. [3]
Природа агрессивной среды, ее агрегатное состояние, химический состав, размеры и конфигурация молекул в значительной степени влияют на интенсивность сорбционно-диффузионных процессов в полимерах. Сорбция органических жидкостей и их паров в полимерах определяется размерами и конфигурацией ее молекул. [4]
Природа агрессивной среды и протекающие при ее контакте с металлами реакции определяют характер процесса коррозии металлов: электрохимический - в электролитах и химический - в сухих газах при высоких температурах или в жидких неэлектролитах. [5]
Конечные продукты коррозии различны в зависимости от природы агрессивной среды; преимущественно это основные соли. [7]
 |
Схема электрохимической коррозии железа с кислородной деполяризацией. [8] |
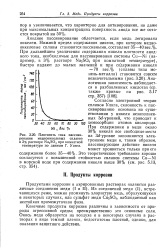
В зависимости от химического состава и структуры металла, природы агрессивной среды, условий ее воздействия электрохимическую коррозию подразделяют на солевую, щелочную, кислотную, атмосферную, почвенную, контактную, биологическую, коррозию под напряжением и пр. [9]
Величина снижения прочности пластрастворов в большей степени зависит от природы агрессивной среды, а также и от наполнителя. [10]
Однако и здесь отмечены оптимальные пределы в зависимости от природы агрессивной среды. Так, например, устойчивость стекла по отношению к кипящей воде остается постоянной при содержании В2О3 до 11 %; при большем содержании В2О3 она быстро понижается. Кипящая НС1 при наличии в стекле до 2 % В2О3, оказывает слабое действие, которое усиливается при повышении содержания В2О3 до 8 % ив дальнейшем становится еще более интенсивным. Аналогично действует и NaOH: вначале слабо, сильнее с увеличением содержания В2О3 до 14 % и значительно сильнее в дальнейшем. [11]
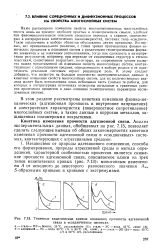 |
Типичные кинетические кривые изменения прочности адгезионной связи в сэндвичевых системах. [12] |
Независимо от природы адгезионного соединения, способа его формирования, природы агрессивной среды и метода определения, характерной особенностью процессов является снижение прочности адгезионной связи, описываемое одним из трех типов кинетических кривых ( рис. 7.13): монотонным изменением А от исходного до некоторого равновесного значения Ааот 5-образными кривыми и кривыми с экстремумами. [13]
 |
Влияние содержания углерода на скорость коррозии сталиХ13 ( термич. обработка. отжиг 850, выдержка в течение 1 часа, охлаждение. [14] |
Коррозионная стойкость нержавеющих сталей определяется устойчивостью пассивной пленки и зависит от природы агрессивной среды. [15]
Страницы: 1 2