Природа - адсорбция
Cтраница 1
Природа адсорбции имеет двоякий характер. Физическая адсорбция основана на действии сил Вандерваальс ( силы притяжения между молекулами реальных газов) и происходит при низких температурах. Помимо физической адсорбции экспериментально установлено при горении углерода наличие химической адсорбции ( хемсорбция), распространяющейся на область более высоких температур. [1]
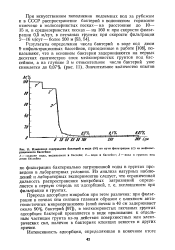 |
Изменение содержания бактерий в воде ( М по пути фильтрации ( L из инфильт-рациоиного бассейна. [2] |
Природа адсорбции микробов при этом различна: при фильтрации в почвах она связана главным образом с влиянием антагонистичных микроорганизмов ( слой почвы в 40 см задерживает около 90 % бактерий [97]), в мелкозернистых песчаных грунтах адсорбция бактерий проявляется в виде прилипания к отдельным частицам грунта из-за действия поверхностных или электрических сил, наличия в бактериях клеящих веществ и других причин. [3]
Природа адсорбции углеводородов на графите, окисях, гидроокисях и химически модифицированных поверхностях. [4]
Поскольку природа адсорбции газов и паров чрезвычайно многогранна и сложна ни одна из существующих теорий не способна объяснить все многообразие явлений адсорбции ( а тем более низкотемпературной адсорбции), хотя при обработке большого числа экспериментов хорошие результаты дает применение теории Лэнгмюра, БЭТ и особенно потенциальной теории. [5]
Для выявления природы адсорбции пленкообразова-телей на пигментах было проведено изучение адсорбции резидрола на исследуемых пигментах весовым методом из водных растворов различной концентрации. [6]
Все сказанное о природе адсорбции водо - и маслорастворимых ПАВ можно отнести и к ПАВ, растворимым в обеих фазах, по крайней мере при их небольших концентрациях. В этом случае в равновесии находятся растворы ПАВ в водной и масляной фазах и адсорбционный слой на межфазной поверхности. [7]
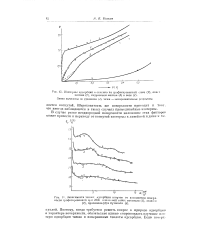 |
Изотермы адсорбции н-гексаяа на графитировапнсш саже ( 7, окиси. [8] |
Поэтому, когда требуется решить вопрос о природе адсорбции и характере поверхности, обязательно нужно сопровождать изучение изотерм адсорбции также и измерениями теплоты адсорбции. [9]
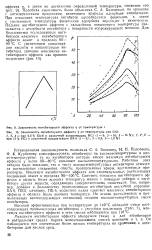 |
Зависимость ингибнторного эффекта v от температуры t.| Зависимость иигнбиторного эффекта v от температуры для СтЗ. [10] |
Подобная зависимость была объяснена БалезиньЛ по аналогии с каталитическими процессами, изменением природы адсорбции ингибиторов. При невысоких температурах ингибитор адсорбируется физически, а затем с увеличением температуры физическая адсорбция переходит в химическую. Падение иигибиторного эффекта с дальнейшим повышением температуры связывается с десорбцией ингибитора с поверхности корродирующего металла. [11]
Согласно Тейлору [29] отсутствие непосредственной связи между адсорбцией и каталитической активностью является следствием двойствен ной природы адсорбции. Адсорбция газов при низких температурах не изменяет конфигурации и активности адсорбированных долекул. Только активированная или химическая адсорбция, наблюдающаяся при сравнительно высоких температурах, влияет на активность адсорбированного газа и каталитическое действие. Определение величины адсорбции при температурах, очень близких к рабочим условиям, дает гораздо более строгую зависимость между адсорбцией и каталитической активностью. [12]
Такой порядок адсорбции ароматических углеводородов также находится в согласии с высказанными в первой части статьи взглядами на природу адсорбции гидратированным силикагелем ароматических углеводородов, проявляющих свойства оснований. [13]
Эти правила подтверждались при хроматографическом разделении олефиновых фракций нефтепродуктов и также подтверждают выводы, сделанные на основании изучения природы адсорбции углеводородов с учетом электронодонорных свойств олефинов. [14]
Для того чтобы сделать выбор между этими тремя возможностями, необходимо располагать дополнительными данными по кинетике реакции, природе адсорбции реагирующих газов и вероятной устойчивости различного рода промежуточных образований. Ниже приводятся доказательства в пользу того, что механизм б применим к обмену насыщенных углеводородов, а механизм в - к обмену многих ненасыщенных углеводородов. [15]
Страницы: 1 2