Природа - группировка
Cтраница 1
Природа группировок при атомах азота гетероостатков обычно оказывает на окраску цианиновых красителей незначительное влияние ( различия в положениях максимума поглощения достигают 8 - 9 тр. [1]
Природа группировки с промежуточным значением р / С, равным 6, оставалась ( и остается до сих пор) неясной. Сама величина р / С 6 может быть отнесена к имидазолу, но вместе с тем она не зависит от температуры, что характерно для карбоксила. Авторы предполагают, что это имидазол с аномальной величиной АЯ ионизации, однако признают, что для окончательного доказательства этого предположения, нужны дополнительные данные. В этой работе были установлены детали механизма действия рибонуклеазы, в том числе обнаружены реакции изомеризации свободного фермента и комплекса фермент: - продукт. Тщательность кинетического анализа, проведенного в этой работе, позволяет отнестись с доверием к предложенному авторами химическому механизму действия рибонуклеазы, хотя не вполне ясно, действительно ли все обнаруженные реакции изомеризации входят в последовательность каталитических реакций. [2]
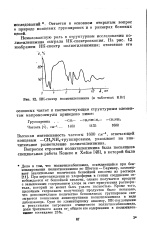 |
ИК-спектр полиэтиленимина ( в таблетках КВг. [3] |
Остается в основном открытым вопрос о природе концевых группировок и о размерах боковых цепей. [4]
Установлен ряд количественных зависимостей гидролитической устойчивости различных полимеров, свидетельствующих о том, что природа боковых группировок в цепи линейных полимеров в значительной степени предопределяет скорость гидролитической деструкции. [5]
Полоса поглощения группы РО имеет среднюю интенсивность, но иногда она меняется в зависимости от природы соседних группировок. Сравнение абсолютных интенсивностей для различных классов веществ осложняется тем, что данная полоса очень часто появляется в виде дублета. Гор [4] первоначально предположил, что вторая из этих полос у этилфоефатов обусловлена колебаниями О - С2Н5, однако наличие дублетного характера полосы у многих полностью ароматических фосфатов и фосфонатов свидетельствует о том, что эта полоса связана с самими колебаниями РО. [6]
В последнее время получено много данных о тонкой структуре углеводной части веществ групп крови и о природе детерминантных группировок. Основными путями исследования явились: изучение инги-бирования агглютинации эритроцитов различными моно - и олигосаха-ридами, ферментативный гидролиз и, наконец, выделение и идентификация фрагментов с антигенной активностью, полученных частичным кислотным гидролизом веществ групп крови. [7]
Полоса поглощения группы Р О имеет довольно сильную интенсивность, но иногда она меняется в зависимости от природы присоединенных группировок. Сравнение абсолютных интенсивностей для различных классов веществ осложняется тем, что данная полоса очень часто появляется в виде дублета. Гор [4] первоначально предположил, что вторая из этих полос у этилфосфатов обусловлена колебаниями О - С2Н 5, однако наличие дублетного характера полосы у многих полностью ароматических фосфатов и фос-фонатов свидетельствует о том, что эта полоса связана с самими колебаниями Р О. Вопрос о природе дублетного характера полосы окончательно еще не решен, но были выдвинуты предположения о взаимодействии группы с близлежащими группами СН [25, 28], возможно также, что здесь сказывается явление поворотной изомерии. [8]
Относительные количества двойных связей в молекулах полиэтиленов BbicoKOJ o и низкого давлений довольно близки, однако имеется отличие в природе группировок, содержащих ненасыщенные связи. [9]
В отличие от полиарилатов, термостойкость которых лимитируется устойчивостью сложноэфирной связи основной цепи, стабильность полиамидов и полиимидов, которые имеют более устойчивые, по сравнению с С-О, C-N связи, в первую очередь, определяется природой кардовой группировки. Согласно данным термогравиметрического анализа, распад полиамидов начинается при 360 - 450 С [66-70], а температуры начала разложения полиимидов [33-34, 71-78] находятся в области 450 - 520 С. [10]
Прочность связи, зависящая от многих факторов ( заряда центрального иона, природы центрального иона и адденда, знака и величины заряда образуемого комплекса, наличия во внутренней сфере циклических группировок, включающих центральный ион, и, наконец, природы внешнесферных группировок) не может быть непосредственно приведена в соответствие с типом связи. [11]
Независимо от механизма участия ионогенных групп фермента в каталитическом эффекте исследование влияния рН на скорость ферментативной реакции позволяет количественно охарактеризо-вать кислотно-основные свойства этих групп, а это, в свою очередь, дает возможность по величине рК в первом приближении идентифицировать природу ионогенных группировок, связанных ( прямо или косвенно) с каталитическим действием. В связи с этим нельзя не согласиться с мнением много работавшего в области ферментативной кинетики Лейдлера [5], что строго количественное исследование влияния рН на скорость энзиматических реакций, может много дать для расшифровкл механизма элементарных стадий этих реакций. [12]
Гидроксильные соединения обычно легко ассоциируются с помощью водородных связей [13] ( см. ниже), и их спектры, следовательно, сильно зависят от состояния образца и природы применяемого растворителя ( ср. Дальнейшее разбавление влиять не должно, и тогда можно составить представление о природе конкретной гидроксильной группировки на основании частоты, ширины и интенсивности полосы ( или полос) поглощения. В особенности большую ценность с этой точки зрения представляет полоса валентного колебания v ( OH), которая широко изучалась, причем было показано, что эта полоса воспроизводима и характеристична. [13]
Сложноэфирные группировки -, в условиях воздействия спиртовой щелочи п последующей обработки соляной кислотой вновь распадаются с образованием свободных карбоксильных групп. Наряду с омылением образовавшихся при метилировании сложноэфпрных групп опыляются и предсуществующие в органическом веществе неизвестные по своей природе группировки. Вследствие этого значительно снижается содержание углерода и соответственно возрастает содержание кислорода. Последующее метилирование омыленного образца действительно показывает увеличение метоксплыюго числа, что свидетельствует об омылении и образования дополнительного количества шдро-ксидышх групп, способных вступать в реакцию с дказометаном. [14]
Идентификация активных красителей на волокне включает решение двух задач: идентификацию хромофорной системы и активной группировки. Обсужденные ранее методы относятся к первой части проблемы и включают обычные способы идентификации какого-либо класса красителей. Установление природы активной группировки, химически связанной с волокном, является более трудной и часто неразрешимой задачей. Методы, предложенные Боде, Иординсоном, Локвудом и другими, основаны на относительной устойчивости связи краситель - волокно к кислотному и щелочному гидролизу. [15]
Страницы: 1 2