Кислотная природа
Cтраница 3
В соответствии с их кислотной природой сульфаниламид ( п-аминобензолсульфамид), сульфадиазин ( 2-сульфаниламинопири-мидин) и другие сульфамидные препараты тоже дают положительную реакцию. Барбитуровая кислота и ее производные, за исключением 5 - нитро5арбитуровой кислоты, тоже дают положительную реакцию. [31]
Все эти свойства указывают на сильно кислотную природу такого раствора. Аналогично раствор амида щелочного металла в жидком аммиаке окрашивает фенолфталеин в красный цвет и осаждает амиды тяжелых металлов из раствора, а это - типичные свойства оснований. [32]
Отравление органическими основаниями указывает на кислотную природу каталитической активности цеолитов. При введении в цео-литный катализатор такого протонсодержащего вещества, как вода ( до 2 %), активность его увеличивается в два раза; дальнейшее повышение количества воды не изменяет активности. [33]
На органической матрице группы, имеющие кислотную природу, по силе значительно отличаются друг от друга. Этот фактор в большой степени влияет на селективность реакций ионного обмена. [34]
В жидком аммиаке ионизированы некоторые вещества, кислотная природа которых почти или совсем нг проявляется в воде. Мало того, в жидком аммиаке становится лабильным водород у некоторых веществ, реагирующих в воде, как слабые основания. Этим вызвано большое разнообразие типов кислот, существующих в жидком аммиаке. [35]
Каталитические превращения тиа-циклогексана и 2-метилтиациклопентана на катализаторах кислотной природы. [36]
Данные по отравлению органическими основаниями указывают на кислотную природу каталитической активности цеолитов. [37]
Это указывает на то, что активность катализаторов кислотной природы определяется числом функциональных групп на их поверхности. [39]
В последующем изложении будут приведены доказательства в пользу кислотной природы веществ, составляющих алюмо-силикатные катализаторы, и того факта, что эта кислотность имеет непосредственное отношение к активности этих катализаторов. Далее будут развиты определенные соображения относительно структуры систем, состоящих из окиси кремния и окиси алюминия, как в состоянии влажного геля, так и в прокаленном состоянии. Будет изложен принцип, коррелирующий известные особенности этих систем, позволяющий дать простую и рациональную картину химической природы алюмосиликатных катализаторов и явлений катионного обмена. Этим принципом является способность алюминиевого иона к обратимой координации. Наконец, будет показано, что присутствие активных ионов водорода ( в бренстедовском смысле) как в гидрогеле, так и в прокаленных составах из окиси кремния - окиси алюминия нежелательно. Механизм некоторых видов каталитического действия, оказываемого катализаторами крекинга, будет обсужден на основании их выясненных химических особенностей. [40]
Как уже было сказано, двуокись кремния обладает кислотной природой. Непосредственно с водой она не реагирует, следовательно, этим путем получить кремневую кислоту невозможно. [41]
Мы уже указывали, что двуокись кремния обладает кислотной природой. Непосредственно с водой она не реагирует, следовательно, этим ny-je M получить кремневую кислоту невозможно. [42]
В отличие от других галогенидов Si ( IV) кислотная природа SiF4 проявляется не только при гидролизе, но и при взаимодействии с основными и амфотерными фторидами. [43]
III, 1198 ] указал на то, что кислотная природа метиленовой группы во флуорене и вместе с тем способность его к конденсации с альдегидами усиливается от присутствия атомов галогена в ядре. Известна также повышенная склонность к конденсациям у 2-нитрофлуорена. Леве-нич и Лезер [ J. II, 1955J экспериментально подтвердили эти наблюдения. Они нашли, кроме того, что в качестве побочного продукта при конденсации образуется красное кристаллическое вещество неизвестного строения. [44]
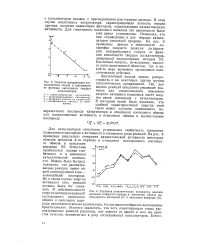 |
Скорость дегидратации изо.| Удельная каталитическая активность окислов., металлов четвертого периода в отношении обмена молекулярного кислорода ( / и окисления водорода ( / /. [45] |
Страницы: 1 2 3 4