Присоединение - кислород
Cтраница 2
Присоединение кислорода к такому радикалу должно дать бирадикал RO2 -, существование которого не доказано. Допустив возможность существования подобных радикалов, можно принять, что их свободные валентности рекомбинируют друг с другом, с образованием насыщенной связи. Однако в случае полимеров атомы со свободными валентностями, находящиеся в одной молекуле, могут отстоять далеко друг от друга, вследствие чего возможность рекомбинации станет малой и радикал типа - RO2 - окажется достаточно устойчивым. [16]
Присоединение кислорода к молекуле углеводорода облегчает дальнейшее ее окисление. Это означает, что разрыв молекулы происходит как по двойным связям, так и по соседним ординарным связям. [17]
Присоединение кислорода к углеводороду не всегда сопровождается деструкцией последнего, и из образующихся перекисных соединений можно восстановлением снова получить исходный углеводород. Реакция же с озоном, повидимому, всегда связана с внедрением атома кислорода в основной углеродный скелет молекулы, так что восстановлением озонидов получить исходные вещества не удается. [18]
Присоединение кислорода к такому радикалу должно дать бирадикал - RO2 -, существование которого не доказано. Допустив возможность существования подобных радикалов, можно принять, что их свободные валентности рекомбинируют друг с другом, с образованием насыщенной связи. Однако в случае полимеров атомы со свободными валентностями, находящиеся в одной молекуле, могут отстоять далеко друг от друга, вследствие чего возможность рекомбинации станет малой и радикал типа - RO - окажется достаточно устойчивым. [19]
Присоединение кислорода к молекуле углеводорода облегчает дальнейшее ее окисление. Это означает, что разрыв молекулы происходит как по двойным связям, так и по соседним ординарным связям. [20]
Присоединение кислорода к углеводороду не всегда сопровождается деструкцией последнего, и из образующихся перекисных соединений можно восстановлением снова получить исходный углеводород. Реакция же с озоном, повидимому, всегда связана с внедрением атома кислорода в основной углеродный скелет молекулы, так что восстановлением озонидов получить исходные вещества не удается. [21]
Присоединение кислорода произошло здесь за чужой счет - Связующая электронная пара принадлежала атому азота. [22]
Присоединение кислорода к диенам в присутствии ряда красителей служит примером, на котором выясняется роль сенсибилизаторов в фотохимических процессах. Эта роль состоит в том, что сенсибилизатор в первую очередь поглощает фотон, переходя на возбужденный уровень St. Интеркомбинационная конверсия переводит его далее на триплет-ный уровень. [23]
Присоединение кислорода может происходить в нем только через разрыв двойной связи в карбониле. [24]
Присоединение кислорода к 1 ( иоизомеру кретоновой кислоты приводит к обоим антиподам эрыгро-формы а р-диоксимасляной кислоты. [25]
Присоединение кислорода сопровождается, очевидно, более или менее сильной деструкцией. Исследование вопроса о характере функциональных групп, в виде которых присоединенный кислород находится в молекулах окисленного каучука, показало [47], что преимущественно он находится в форме эпоксидных или эфирных группировок, но может также образовывать и гидроксильные группы. [26]
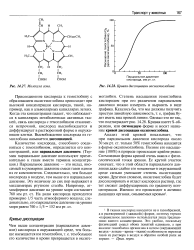 |
Молекула гема.| Кривая диссоциации оксигемоглобина. [27] |
Присоединение кислорода к гемоглобину с образованием оксигемоглобина происходит при высокой концентрации кислорода, такой, например, как в альвеолярных капиллярах легких. Когда эта концентрация падает, что наблюдается в капиллярах метаболически активных тканей, связь кислорода с гемоглобином становится непрочной, кислород высвобождается и диффундирует в растворенной форме в окружающие клетки. Высвобождение кислорода из гемоглобина называется диссоциацией. [28]
Присоединение кислорода к концам ненасыщенной молекулы наблюдается не только в случае конъюгированных диенов. [29]
Поэтому присоединение кислорода к комплексу МА, в котором М обладает электронной конфигурацией d или d, сопряжено с формальным окислением ком-плексообразователя и расширением его координационной сферы. [30]
Страницы: 1 2 3 4