Присоединение - лиганд
Cтраница 2
Как отмечалось ранее, эти скачки можно объяснить только тем, что вероятность присоединения лигандов не одинакова для всех координационных положений. [16]
Замещение лигандов первой координационной сферы металла лигандными группами ионита не отрицает и ассоциативный механизм присоединения лигандов ионита к иону металла, поскольку в процессе его диффузии в грануле ионита могут произойти значительные изменения состава координационной сферы. [17]
Координационные комплексообразова-тели - соли металлов переходной валентности - способны выполнять функции гетерогенных катализаторов для многочисленных реакций присоединения возможных лигандов к ненасыщенным углеводородам или реакций, протекающих через стадию такого присоединения. [18]
Данный метод применим для определения состава и констант нестойкости комплексов, если полосы поглощения, вызванные присоединением лигандов и металла, не накладываются друг на друга или могут быть разложены на гауссовские компоненты. Число полос поглощения или гауссовских компонентов в этом случае соответствует числу существующих в растворе комплексов. Концентрация комплексов в растворе определяется фотографическим способом при регистрации спектров поглощения на фотопластинке. [19]
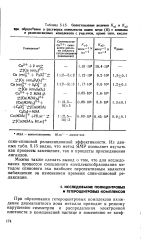 |
Сопоставление величин Кз1 и Ks2. [20] |
Из данных табл. 5.15 видно, что метод ЯМР позволяет изучать как процессы замещения, так и процессы присоединения лигандов. [21]
Однако если в первых двух ионах бидентатная координация металла группами МО3 симметрична, то в [ Со ( МО3) 4р - она асимметрична, хотя в двух группах NO3 длины двух разных связей Со-О составляют 2 03 и 2 36 А, в то время как в двух других - 2 11 и 2 54 А. Впрочем следовало бы отметить, что асимметричное присоединение лигандов МОз наблюдается также и в ионе [ Zn ( NO3) 4 ] 2 -, причем более длинным связям с Zn соответствуют более короткие связи N-О и наоборот. [22]
 |
Схемы уровней энергии d - орбиталей центрального иона для комплексов различной конфигурации. [23] |
На рис. 2.4 схематически показаны уровни энергии d - орбиталей для комплексов различной структуры. Чтобы избежать недоразумений, следует напомнить, что при присоединении лигандов к иону в газообразном состоянии общая энергия системы уменьшается. Однако вследствие отрицательного заряда лигандов энергия всех d - орбиталей должна увеличиться. Энергия некоторых d - орбиталей увеличивается больше, чем других. Таким образом, каждая структура, указанная на этом рисунке, имеет свое собственное абсолютное значение энергии, которое не может быть связано с энергиями соседних конфигураций. [24]
Однако нелинейность стационарной кинетики в этих случаях никак не означает удаленности системы от состояния равновесия - она возникает и при равновесных соотношениях фермента с ли-гандами. В модели Моно, Уаймана и Шанже ( модель МУШ) [9, 50, 51] присоединение лигандов приводит лишь к сдвигу равновесия. [25]
Как правило, константы ассоциации при ступенчатом образовании комплекса ( уравнение 11.20) имеют тенденцию к уменьшению по мере увеличения числа лигандов. Эта тенденция обычно проявляется особенно сильно в тех случаях, когда основная форма лиганда несет суммарный заряд ( пример - кислородсодержащий аннон), так как присоединение последующих лигандов приводит к возникновению между лигандами постепенно возрастающего электростатического отталкивания. [26]
Ионы металлов Pt2, Pd2, Au3 и Cu2 образуют почти исключительно плоские квадратные структуры, в то время как для Ni2, Co2, Fe2 и Мп2 структуры этого типа вообще встречаются гораздо реже и в приведенном ряду металлов распространенность плоских структур снижается. В ковалентных плоских квадратных хелатах этих металлов предпочтительна конфигурация со спаренными электронами ( - гибридизация), поэтому они представляют собой диамагнитные соединения, например бис - ( диметилглиоксимато) никель. Для комплексов этого типа менее характерно присоединение дополнительных лигандов, таких, как пиридин или аммиак, с образованием октаэдрических структур. И наоборот, полярный, тетраэдрический парамагнитный бис - ( ацетилацето-нато) никель очень легко реагирует с пиридином, образуя октаэдриче-ский аддукт. [27]
Электролитическая диссоциация комплексных кислот и оснований позволяет характеризовать их как сильные электролиты даже в том случае, если лиганды образуют с ионами Н или ОН очень слабодиссоциированные кислоты или основания. Например, HF - слабая кислота, H [ BF4 ] - сильная; HCN - слабая кислота, H [ Ag ( CN) 2 ] - сильная. Это объясняется увеличением объема аниона или катиона в результате присоединения лигандов и ослаблением кулоновского взаимодействия между внутренней и наружной сферами. [28]
Это обусловлено малой величиной их радиусов и значительной поляризуемостью, сьязанной с наличием во внешнем слое uf - электронов. Особенно много комплексов известно для Соь, что объясняется прочностью присоединения лигандов к данному иону. [29]
При выборе спейсера, помимо длины, следует учесть степень его гидрофобности, поскольку от этого может зависеть неспецифическая сорбция на матрице. Необходимо также выбрать химическую группу, которая окажется на свободном конце спейсера; к этой группе должен присоединяться лиганд. Что касается присоединения спейсера к матрице, то здесь используются те же приемы, какие были описаны для присоединения лигандов к активированным матрицам, поэтому на ближайшем к матрице конце спейсера почти всегда располагается аминогруппа. [30]
Страницы: 1 2 3