Присоединение - метилен
Cтраница 2
Двустадий-ный синтез циклопропанов путем присоединения дигалокарбена и восстановления предпочитают присоединению метилена, поскольку в этом случае не оэразуется продуктов внедрения. Однако этот метод может оказаться хуже, чем каталитические реакции ( СиС12, ZnX2, R2A1X) диазометана с олефинами ( ср. [16]
Эта реакция с диазометаном не является избирательной, поэтому вероятность присоединения метилена к различным связям С - Н определяется их относительным количеством, и состав образующихся продуктов может быть предсказан заранее. [17]
 |
Устройство для получения диазометана. [18] |
В связи с тем, что реакция метиленирования не является избирательной реакцией и вероятность присоединения метилена к различным связям С - Н определяется только концентрацией этих связей в молекуле реагирующего углеводорода, то качественный состав и количественное распределение образующихся продуктов могут быть определены расчетным путем. В продуктах метиленирования н-пентана было найдено 50 % н-гексана, 34 % 2-метилпентана и 1 % 3-метилпентана в полном соответствии с теорией. [19]
В настоящее время считают, что при этом происходит внедрение метилена в связи С - Н, но раньше думали, что имеет место присоединение метилена к свободной электронной паре кислорода. Образующийся при этом илид ( VIII) далее подвергается перегруппировке. [20]
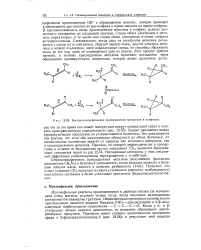 |
Нестер еоспецифическое присоединение метиленов к олефинам. [21] |
ОН с образованием эпокиси, которое приводит к образованию ис-эпокиси из г ис-олефина и / пранс-эпокиси из транс-олефина. В противоположность этому присоединение метилена к олефину должно происходить постадийно по следующей причине. Спины обоих электронов в метилене параллельны, в то время как спины обоих электронов я-связи олефина антипараллельны. Следовательно, когда один из электронов метилена связывается с одним из я-электронов, образуя первую связь, другой электрон метилена и второй я-электрон, имея параллельные спины, не способны образовать связь до тех пор, пока не перевернется один из спинов. [22]
Многие циклопропановые системы были изучены Кистяков-ским, Фреем, Рабиновичем и их сотрудниками. Наиболее интересным было исследование метилциклопропана, который мсжет образовываться двумя путями [11]: либо при присоединении метилена к пропилену, либо путем внедрения Метилена по С - Н - связи циклопропана. Образующиеся таким образом молекулы метилциклопропана различаются по содержанию энергии на 8 ккал / молъ, что соответствует разности в теплотах образования пропилена и циклопропана. Содержание энергии можно варьировать, используя метилен, полученный из кетона и пиазометана при освещении их светом с различными длинами волн. Было получено шесть видов метилциклопропана с различным содержанием энергии и измерены скорости их изомеризации. Сильной стороной этой методики является возможность выбора модели изомеризации, основанной на результатах опытов по термической изомеризации при низких давлениях, и возможность проверки справедливости модели путем вычисления содержания энергии у всех шести типов образованных молекул. Можно было бы полагать, что в принципе возможно получать метилциклопропан с совсем другим содержанием энергии при реакции бирадикала СН3СН: с этиленом. Этилидеи является гораздо менее реакционноспособным по отношению к присоединению, чем метилен, так что, вероятно, трудно найти подходящие условия для синтеза. [23]
Многие циклопропановые системы были изучены Кпстяков-ским, Фреем, Рабиновичем и их сотрудниками. Наиболее интересным было исследование метилциклопропана, который может образовываться двумя путями [ И ]: либо при присоединении метилена к пропилену, либо путем внедрения метилена по С - Н - связи циклопропана. Образующиеся таким образом молекулы метилциклопропана различаются по содержанию энергии на 8 ккал / молъ, что соответствует разности в теплотах образования пропилена и циклопропана. Содержание энергии можно варьировать, используя метилен, полученный из кетона и диазометана при освещении их светом с различными длинами волн. Было получено шесть видов метилциклопропана с различным содержанием энергии и измерены скорости их изомеризации. Сильной стороной этой методики является возможность выбора модели изомеризации, основанной на результатах опытов по термической изомеризации при низких давлениях, и возможность проверки справедливости модели путем вычисления содержания энергии у всех шести типов образованных молекул. Можно было бы полагать, что в принципе возможно получать метилциклопропан с совсем другим содержанием энергии при реакции бирадикала СН3СН: с этиленом. Этилиден является гораздо менее реакционноспособным по отношению к присоединению, чем метилен, так что, вероятно, трудно найти подходящие условия для синтеза. [24]
В результате реакций метилена ( синглет) с олефинами и алканами возникают богатые энергией молекулы, которые претерпевают затем множество нерадикальных превращений. Метилен получали в результате фотолиза ( 4100 А) и термического распада диазометана, а также фотолиза кетена при длинах волн, больших и меньших 3100 А. Присоединение метилена по двойной связи является сте-реоспецифическим. [25]
Опыты по термической изомеризации [14] показывают, что энергия активации уменьшается приблизительно на 4 5 ккал / молъ для каждого атома фтора, который введен в молекулу. С другой стороны, результаты, полученные при низких давлениях, показывают, что эффективное число осцилляторов Касселя увеличивается на два для каждого атома фтора. Таким образом, оказывается, что для молекул с энергией приблизительно 112 ккал / молъ, полученных при присоединении метилена, два фактора - более низкая энергия активации и увеличение эффективной сложности - почти полностью компенсируют друг друга. Для полного анализа результатов этой интересной серии исследований необходимы термохимические данные для реагентов и продуктов реакции. [26]
Все продукты, представленные в уравнениях ( 39) - ( 41), образуются при изомеризации горячего винилциклопропана. В случае термической изомеризации винилциклопропана ( при температуре около 370) основным продуктом является циклопентен, а других диенов получены лишь следы. Это обусловлено тем, что реакции, приводящие к этим другим продуктам, имеют более высокие энергии активации, и этой разницы достаточно, чтобы подавить их почти полностью. Однако если возбужденный винилциклопропан образовался в результате присоединения метилена, то это различие в энергии играет значительно меньшую роль, и поэтому изомеризуется с образованием диенов примерно столько же молекул, сколько превращается в циклопентен. [27]
Метилен получали облучением как диазометана, так и кетена при различных суммарных давлениях как в присутствии, так и в отсутствие добавок инертных газов. Отношение выхода изомеров бутилена к выходу метшщиклопропа-на уменьшалось с увеличением давления, причем при любом источнике метилена результаты находились в соответствии с законом скорости реакции, выведенным в предположении, что изомеризация горячего метилциклопропана конкурирует с охлаждением его вследствие столкновений с другими молекулами. Так как выход изомеров бутилена в случае метилена, полученного из диазометана, был больше, чем в случае кетена в сравнимых условиях, Ки-стяковский сделал вывод, что метилен образовывался из диазометана в сравнительно более высоком состоянии возбуждения. При этом предполагалось, что избыточная энергия является в основном поступательной, так как эти результаты можно было объяснить только допущением, что охлаждение и реакция с циклопропаном имеют близкие константы скорости. Очевидно, что циклопропаны, получающиеся в результате присоединения метилена к двойным связям, также должны быть в возбужденном состоянии как вследствие экзотермичности реакции присоединения, так и вследствие возбуждения: СНа в процессе реакции. [28]
Кажется, что очевидная интерпретация этих результатов говорит в пользу предположения Скелла. Сенсибилизированные реакции должны приводить к триплетному метилену, а прямое облучение, как известно, дает синглетный метилен. При высоком давлении инертного газа синглетный: СН2 может переходить в триплетное состояние прежде, чем прореагирует с ненасыщенным субстратом. Однако такая ясная на первый взгляд картина становится значительно более сложной при внимательном критическом анализе. Прежде всего, первое предположение Скелла следует рассматривать как результат интуиции, а не как надежную теорию. Нет никаких твердых оснований считать, что вращение вокруг простых связей обязательно будет происходить быстрее, чем инверсия спина. Последний процесс является медленным по сравнению с про-должительностями излучательных переходов, но не представляется надежно отнесенным на шкале времени большинства физических событий. С другой стороны, совсем не обязательно, что присоединение синглетного метилена к двойной связи должно быть одностадийным процессом именно потому, что оно могло бы осуществиться без нарушения сохранения спина. Следовательно, можно легко представить себе как стереоспецифичное присоединение триплетного карбена, так и нестереоспецифичное синглетное присоединение. Наконец, как уже четко указал Фрей [80], циклопропан, полученный присоединением синглетного метилена к алкену с сохранением энергии, был бы достаточно горячгш для участия в различных реакциях изомеризации, если бы он быстро и эффективно не дезактивировался. Почти не рискуя впасть в ошибку, можно сказать, что согласно наиболее распространенному мнению второе предположение Скелла, как и первое, оказалось правильным. Однако Де Мор и Бенсон [51 ] приняли ту точку зрения, что всю химию присоединения метилена можно объяснить, исходя из синглетного спинового состояния, если правильно учесть, каким образом энергия возбужденного метилена и промежуточных соединений передается другим окружающим молекулам. Хотя этот довод кажется мало убедительным, все же он будет внимательно рассмотрен здесь. [29]
Страницы: 1 2