Присоединение - гидроперекись
Cтраница 1
Присоединение гидроперекисей к непредельным простым эфирам протекает в присутствии кислых катализаторов, например хлористого водорода, в эфире. [1]
Присоединение гидроперекиси к метилэтилкетону происходит при 80 С сравнительно медленно, но ускоряется добавками органических кислот, например, уксусной. Таким образом, взаимодействие гидроперекисей с кетонами, приводящее к ускоренному образованию свободных радикалов, по-видимому, играет существенную роль в механизме окисления цикло-гексана, вторичных спиртов и кетонов. При окислении парафиновых углеводородов взаимодействие кетонов с гидроперекисями не изменяет скорости инициирования цепей, так как концентрации кетонов, накапливающихся в ходе процесса, меньше тех концентраций, при которых заметно влияние кетонов. [2]
Присоединение гидроперекисей к непредельным простым эфирам протекает в присутствии кислых катализаторов, например хлористого водорода, в эфире. [3]
Присоединение гидроперекиси к метилэтилкетону происходит при 80 С сравнительно медленно, но ускоряется добавками органических кислот, например, уксусной. Таким образом, взаимодействие гидроперекисей с кетонами, приводящее к ускоренному образованию свободных радикалов, по-видимому, играет существенную роль в механизме окисления цикло-гексана, вторичных спиртов и кетонов. При окислении парафиновых углеводородов взаимодействие кетонов с гидроперекисями не изменяет скорости инициирования цепей, так как концентрации кетонов, накапливающихся в ходе процесса, меньше тех концентраций, при которых заметно влияние кетонов. [4]
Примером присоединения гидроперекиси к активированной двойной связи является реакция метилгидроперекиси с виниловыми эфирами в присутствии п-толуолсульфокислоты или трех-фтористого бора. [5]
Скорость присоединения гидроперекисей к различным карбо - нильным соединениям уменьшается при введении электронодо-норных заместителей по соседству с карбонильной группой. Это показывает, что нуклеофильный реагент - гидроперекись - в лимитирующей стадии процесса атакует электрофильный центр карбонильной группы. [6]
Примером присоединения гидроперекиси к активированной двойной связи является реакция метилгидроперекиси с виниловыми эфирами в присутствии п-толуолсульфокислоты или трех-фтористого бора. [7]
Скорость присоединения гидроперекисей к различным карбонильным соединениям уменьшается при введении электронодо-норных заместителей по соседству с карбонильной группой. Это показывает, что нуклеофильный реагент - гидроперекись - в лимитирующей стадии процесса атакует электрофильный центр карбонильной группы. [8]
Гидроперекиси и продукты присоединения гидроперекисей избирательно взаимодействуют с сернистым ангидридом реактива Фишера таким же образом, как взаимодействует перекись водорода ( см. гл. [9]
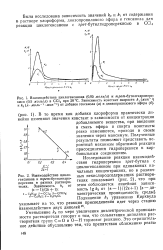 |
Взаимодействие циклогексанона и / пр. т-бутилгидро-перекиси в разных растворителях. Зависимость 62 от. [10] |
Полученные результаты позволяют представить вероятный механизм обратимой реакции присоединения гидроперекиси к карбонильным соединениям. [11]
Полученные результаты позволяют представить вероятный механизм обратимой реакции присоединения гидроперекиси к карбонильным соединениям. [13]
Эти различия в реакционной способности циклических кетонов находятся в соответствии с константами скоростей реакций присоединения гидроперекисей к кетонам, которые уменьшаются в ряду: циклогексанон 4-метилциклогексанон 3-метилциклогексанон. [14]
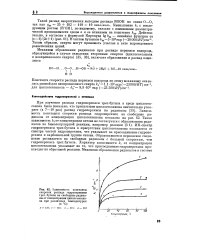 |
Зависимость константы скорости распада гидроперекиси трет, бутила на свободные радикалы от концентрации циклогексанона при различных температурах ( в С. [15] |
Страницы: 1 2
