Присутствие - ион - аммоний
Cтраница 3
Лакмусовая бумага может быть заменена фильтровальной бумагой, смоченной реактивом Несслера. В присутствии ионов аммония такая реактивная бумага окрашивается в желтый или коричневый цвет. [31]
Реакцию проводят так: в пробирку с испытуемой солью или раствором вводят раствор щелочи и смесь осторожно нагревают. В присутствии иона аммония выделяется аммиак. [32]
Образовавшуюся мутную смесь, содержащую аморфный фосфат магния, помещают в газовую камеру, на дне которой находится капля исследуемого раствора, обработанная раствором едкого натра. В присутствии иона аммония в капле смеси реактивов образуются характерные кристаллы двойного фосфата в виде трапеций и прямоугольных призм, напоминающих крыши домов. [33]
На фильтровальной бумаге выполняют пробу следующим путем: каплю фильтрата, полученного после обработки исследуемого раствора концентрированной едкой щелочью, помещают на фильтровальную бумагу, и в центр влажного пятна вносят каплю реактива Несслера. В присутствии иона аммония появляется желтое или оранжевое пятно или кольцо. [34]
Реакцию проводят так: в пробирку с испытуемой солью или раствором вводят раствор щелочи и смесь осторожно нагревают. В случае присутствия иона аммония выделяется аммиак. [35]
Реакцию проводят так: в пр Эбирку с испытуемой солью или раствором вводят раствор щелочи и смесь осторожно нагревают. В случае присутствия иона аммония выделяется аммиак. [36]
Это указывает па отеутствче в течение этого времени процесса перекристаллизации твердой фазы. Из этого следует, что присутствие ионов аммония в растворе заметно увеличивает продолжительность существования днгидрата дикальциифосфата. [37]
Почти все остальные катионы не мешают открытию натрия. Так, можно открыть натрий в присутствии ионов аммония, калия, бария, стронция, кальция, магния, алюминия, хрома, железа, кобальта, никеля, марганца, ртути, свинца, висмута, кадмия и меди, если эти катионы присутствуют в растворе в 20-кратном количестве по сравнению с ионом натрия. [38]
Эта реакция отличается высокой чувствительностью. NaOH, что позволяет открывать ионы калия в присутствии ионов аммония без их предварительного удаления. [39]
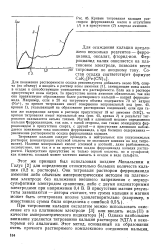 |
Кривые титрования кальция раствором ферроцианида калия в отсутствие ( 1 и в присутствии ( 2 хлорида аммония. [40] |
Для понижения растворимости осадка рекомендуется добавлять около 60 % спирта ( по объему) и вводить в раствор ионы аммония [1], замещающие ионы калия в осадке и способствующие уменьшению его растворимости. Если же в растворе присутствуют ионы натрия, то присутствие ионов аммония обязательно, так как они препятствуют образованию более растворимого кальций - натрий ферроцианида. Например, если в 20 мл титруемого объема содержится 70 мг натрия ( Na), то кривая титрования имеет совершенно неправильный ход ( рис. 45, кривая 1), указывающий на образование растворимых соединений; если при таком же содержании натрия в растворе присутствует 18 мг аммония ( NHJ), то кривая титрования имеет нормальный вид ( рис. 45, кривая 2) и результат титрования оказывается весьма точным. Магний и алюминий мешают определению кальция 1рерроцианидом, так как, с одной стороны, они также осаждаются фер-роцианидом в присутствии спирта, с другой - в присутствии алюминия наблюдается понижение тока окисления ферроцианида, а при больших содержаниях - увеличение растворимости осадка ферроцианида кальция. [41]
Гидроокись марганца Мп ( ОН) 2 выпадает в виде белого осадка при обработке раствора соли марганца ( II) щелочью. Аммиак лишь частично осаждает гидроокись марганца, а в присутствии ионов аммония осадок совершенно не образуется ( сходство с гидроокисью магния) ( см. стр. На воздухе осадок гидроокиси марганца быстро буреет вследствие окисления. Он имеет такую же кристаллическую решетку, как и Mg ( OH) 2 ( стр. Основные свойства гидроокиси марганца слабо выражены, и в этом отношении она похожа на гидроокись магния. [42]
Поэтому необходимо изыскать условия улучшения кристаллизации гипса из загрязненных фосфорнокислых растворов и ускорения их фильтрации. Одним из путей в этом направлении является осуществление экстракции фосфорной кислоты в присутствии ионов аммония, другим - раздельное выделение из раствора полу торных окислов и магнийаммонийфосфата, осажденных в опта-мальных условиях, по так называемой магнийаммонийфосфатной схеме переработки магнийсодержащих фосфоритов. [43]
В некоторых случаях, например, при декоративном цинковании, а также при нанесении защитного покрытия на изделия из чугуна, литья, высокоуглеродистых сталей, целесообразно применение слабокислых электролитов. Однако высокая агрессивность хлор-ионов, снижение эффективности очистки сточных вод от ионов тяжелых металлов в присутствии ионов аммония ограничивают область применения как хлоридных, так и аммиакатных электролитов. В случае, если предъявляются повышенные требования к пластичности осадков, то лучше применять безаммонийные хлоридные растворы. [44]
 |
Окисление этилового спирта на платиновом аноде. [45] |
Страницы: 1 2 3 4