Присутствие - ион - металл
Cтраница 3
Однако, если распад гидроперекиси протекает в гетерогенной среде ( что всегда имеет место при синтезе привитых сополимеров целлюлозы и ее эфиров), часть гидроперекисных групп даже в присутствии ионов металлов переменной валентности распадается с образованием радикалов ОН. [31]
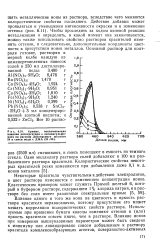 |
Кривые, показывающие влияние диспергатора - лигнинсульфо-ната на раствор Дисперсного желтого 54 в смеси воды с ДМА. [32] |
Чтобы проследить за ходом целевой реакции металлизации и определить, в какой момент она заканчивается, можно также использовать свойство растворов красителей изменять оттенок, и следовательно, дополнительные координаты цветности в присутствии ионов металлов. [33]
Хотя замена нативно-связанного иона металла на тяжелый атом с большей рассеивающей способностью остается привлекательным методом получения производных, содержащих тяжелые металлы, по сравнению с методом проб и ошибок, требующим больших затрат времени [51], тем не менее для белков, активных в присутствии иона металла, желательно no - возможности избегать применения этого метода. Поскольку точное описание стереохимии металл-лигандного координационного центра, существенного для биологической функции белка, является основной целью структурного анализа, всегда предпочтительнее использовать тяжелые металлы, связанные с другими частями белка, или во время приготовления соответствующих производных, или при окончательном расчете соответствующей части карты Фурье. [34]
В частности, из этих работ следует, что во всех случаях нуклеофильная атака на атом фосфора одной из концевой фосфатных групп АТФ независимо от того, выступает ли в качестве нуклеофильного реагента ионизированная оксигруппа кислоты или спирта, или меркаптогруппа КоА, реакции с участием киназ, как правило, требуют присутствия ионов металлов. [35]
Таким образом, вышерассмотренные данные по строению, механизму действия и роли ферментов, гидролизующих фосфорор-ганические ингибиторы холинэстераз, действительно в какой-то степени могут служить подтверждением ранее высказанного предположения о том, что одной из причин крайне медленного дефос-форилирования холинэстераз является недостаточно выраженная электрофильная атака в пуш-пульном механизме нуклеофильного замещения у тетраэдрического атома фосфора в активных центрах эстераз и что присутствие ионов металлов в активных центрах ферментсв способствует переносу фосфорильного остатка на молекулу воды. [36]
Однако прирН 12 образования этих продуктов не происходит. В присутствии ионов металлов, образующих труднораствсГримые сульфиды, скорость разложения комплекса увеличивается. [37]
Важную вспомогательную роль в образовании ферментно-субстрат-ного комплекса играют ионы металла. В частности, присутствие ионов металла необходимо для проявления активности пептидаз. Карбоксипеп-тидаза, полученная из сока поджелудочной железы, содержит цинк. Цинк связан с белком относительно прочно и лишь медленно удаляется при диализе. Полученный после отделения цинка белок неактивен, но полностью восстанавливает активность при добавлении ионов цинка. Особенно интересно то, что в этом случае можно восстановить пептидаз-ную активность ( по отношению к карбобензоксиглицил 1-фенилаланину) не только при помощи цинка, но и посредством ионов других металлов, причем кобальт и никель дают комплексы более активные, чем цинк, а марганец и железо - менее активные. По отношению к различным пептидным субстратам порядок расположения ионов по величинам активностей соответствующих комплексов также оказывается различным. Аналогичный случай мы наблюдали при исследовании модельных соединений, содержащих основания Шиффа, комплексносвязанные с различными металлами. [38]
Синтез макроциклов, включающий построение реагентов вокруг иона переходного металла, может быть основан на координационной геометрии для сближения концов цепи полидентатного лиганда с тем, чтобы они прореагировали с закрывающим цикл фрагментом. Реакция проходит в присутствии иона металла. [39]
Приведенные здесь формы составляют только часть всех возможных; комплексов. Вследствие этого в присутствии ионов металлов нескольких типов устойчивости различных комплексов почти совпадают, а это приводит к тому, что хроматографическое разделение комп-лексообразующих ионов посредством вымывания разбавленными минеральными кислотами является, разумеется, более трудной задачей, чем разделение на монофункциональной иминодиуксусной смоле, а иногда вообще становится невозможным ( ср. [40]
Принцип комплексометрического титрования состоит в следующем. В растворах индикаторы в присутствии ионов металлов образуют неустойчивые окрашенные комплексные соединения, окраска которых отличается от окраски свободных индикаторов. [41]
Форма кривых потенциометрического титрования в неводных средах зависит от используемого электрода, растворителя, фонового электролита и силы кислот или оснований. На форму кривых влияют также присутствие ионов металлов, ассоциация между растворенным веществом и растворителем, образование комплексов кислота - анион кислоты и другие факторы. [42]
Пиридоксаль выполняет функции электрофильного ферментативного катализатора рацемизации а-аминокислот. Эта реакция также ускоряется в присутствии ионов металлов. Как можно заключить на основании схемы (7.32), рацемизация сопровождается реакцией трансаминирования. В системе пиридок-саль - аланин - алюминий рацемизация и трансаминирование конкурируют при всех значениях рН, но при рН 9 6 и 5 доминирующими становятся рацемизация и трансаминирование соответственно. Рацемизацию можно рассматривать просто как образование имина, который уже не располагает асимметрическим центром, а регенерация исходной аминокислоты должна приводить к рацемической смеси. [43]
Фермент карбоангидраза катализирует реакцию гидратации альдегидов, сложных эфиров, а также и двуокиси углерода. Для проявления ее ферментативной активности необходимо присутствие иона металла, например цинка. [44]
 |
Электронные переходы в амиднои [ IMAGE ] Волновые функ-группе ции амиднои группы. [45] |
Страницы: 1 2 3 4