Присутствие - ион - натрий
Cтраница 2
Экспериментальная проверка теории проведена на примере сорбции катионитом КБ-2Х7 катионов аммония и гидроксиламина в присутствии ионов натрия. Полученное уравнение изотермы сорбции слабого основания удовлетворительно подтверждается опытом. [16]
Продукт, выпускаемый фирмой Альберт 82, представляет собой волокнистую массу, образующую в присутствии ионов натрия вязкие растворы. В этих растворах калиймета-фосфат находится в виде полимера ( вероятно, октаметафосфат) и отличается коллоидными свойствами, близкими к свойствам моющих веществ. [17]
Кривые / / и / / / на рис. 3 соответствуют нейтрализации этилендиаминтетрауксусной кислоты в присутствии ионов натрия и лития. Из них видно, что присутствие этих ионов никак не влияет на нейтрализацию двух первых ионов водорода. [18]
Выводы Кейтза и Туттла [309] подтверждены исследованиями Сабатье и Вияра [311], которые показали на синтетическом кварце, что присутствие иона натрия повышает температуру ( 3-а-превра - щения кварца на 7 и сопровождается понижением а0 на 0 0015кХ, тогда как величина ребра ячейки с0 остается без изменений. [19]
Однако присутствие карбоний-ионов в фенолах и жидкой двуокиси, серы давно уже было доказано тем же способом, что и присутствие ионов натрия в воде-электропроводностью и электролизом [21], а также при помощи весьма характерного спектра. При этом, конечно, выяснилось, что везде, где в процессе реакции возникают или исчезают, распространяются или сокращаются ионные заряды, можно наблюдать фантастическую зависимость скорости реакции от растворителя. При неионных реакциях такое изменение растворителей может вызвать ( а может и не вызвать) изменение скорости не более чем в 3 раза. [20]
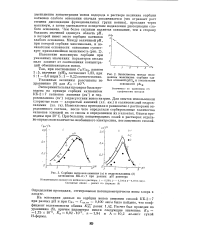 |
Зависимость между положением максимума сорбции слабых основаий ( рН м и показателем основности рКв.| Сорбция катионов аммония ( а и гидроксиламина ( б катионитом КБ-2Х7 при разных рН раствора. [21] |
Экспериментальная проверка была проведена на примере сорбции катионитом КБ-2Х7 катионов аммония ( ам) и гид-роксиламина ( га) в присутствии ионов натрия. [22]
Образование каталитического комплекса с ионами калия приводит, по-видимому, к более благоприятному ослаблению связей в графите, и процесс идет с большей скоростью, чем в присутствии ионов натрия. Кроме указанных причин, ограничивающих применение гидроксида натрия, нужно учитывать его повышенную гигроскопичность и летучесть, ухудшающие условия труда и санитарно-гигиеническую обстановку. [23]
Соосаждение солей щелочных металлов и сульфата аммония увеличивается с увеличением их концентраций и уменьшается с увеличением скорости осаждения и времени созревания осадка. Присутствие ионов натрия в больших концентрациях мешает определению, ионы калия даже при относительно небольших содержаниях вызывают ошибки вследствие их соосаждения. В случае присутствия ионов натрия быстрое прибавление хлорида бария уменьшает соосаждение сульфата натрия. [24]
Летучие соли лития окрашивают бесцветное пламя горелки в характерный карминово-красный цвет. Присутствие ионов натрия маскирует окраску, которая становится при этом нехарактерной. [25]
 |
Кристаллы Na [ Sb ( OH6 ]. [26] |
Подобным же образом ведут себя и кат-ионы 2 - й группы. Появление белого кристаллического осадка служит признаком присутствия иона натрия. При очень малых концентрациях последнего осадок сразу не образуется. В таких случаях, необходимо дать раствору постоять несколько часов. [27]
Хлопьевидный осадок не может служить доказательством присутствия иона натрия, так как это может быть осадок метасурьмяной кислоты, если среда кислая. Он хорошо оседает на дно пробирки и частично пристает к ее стенкам. [28]
К 5 - 8 каплям нейтрального или слабощелочного раствора ( рН 7 5 - 8) приливают 5 - 8 капель раствора KH2SbO4 и потирают о стенки пробирки стеклянной палочкой. Хлопьевидный осадок не может служить доказательством присутствия ионов натрия, так как это может быть осадок метасурьмяной кислоты, если среда кислая. [29]
К 5 - 8 каплям нейтрального или слабощелочного раствора ( рН 7 5 - 8) приливают 5 - 8 капель раствора KH2SbO4 и потирают о стенки пробирки стеклянной палочкой. Хлопьевидный о садок не может служить доказательством присутствия ионов натрия, так как это может быть осадок метасурьмяной кислоты, если среда кислая. Он хорошо оседает на дно пробирки и частично пристает к ее стенкам. [30]
Страницы: 1 2 3