Присутствие - ион - бром
Cтраница 2
На рис. 32, наряду с электрокапиллярными кривыми для электролитов типа KNOs, приведены также кривые, отвечающие тем случаям, когда в растворе присутствуют ионы Br -, I, S2, T1 1, N ( CsH7) J или молекулы амилового спирта. Присутствие ионов брома, иода или серы смещает максимум злектрокапиллярной кривой в сторону более отрицательных. При достаточно отрицательных потенциалах эффект этих анионов исчезает и электрокапиллярные кривые сливаются друг с другом. [16]
Присутствие ионов брома, иода или серы смещает максимум электрокапиллярной кривой в сторону более отрицательных значений потенциалов и ( особенно в области потенциалов, расположенных слева от точки максимума) уменьшает поверхностное натяжение. При достаточно отрицательных потенциалах эффект этих анионов исчезает и электрокапиллярные кривые сливаются друг с другом. Присутствие ионов таллия или ионов тетрабутиламмония сдвигает максимум электрокапиллярных кривых в сторону более положительных значений и уменьшает поверхностное натяжение, особенно заметно при потенциалах, более отрицательных, чем потенциал точки максимума. По достижении достаточно положительных потенциалов, эффект этих катионов исчезает. Присутствие амилового спирта, изменяет форму элект-ро Капиллярной кривой главным образом в области потенциалов, примыкающих к потенциалу максимума. С удалением в обе стороны от потенциала электрокапиллярного максимума эффект добавки амилового спирта снижается и кривая, снятая с добавкой спирта, совпадает с кривой для чистого раствора. [17]
Родий в слабых солянокислых растворах ( до 2 % по объему) не взаимодействует с каломелью, однако из растворов, содержащих 20 % ( по объему) соляной кислоты, можно добиться его количественного выделения. Присутствие ионов брома ( 5 - 7 5 г бромистого калия на 10 мг металла) в растворе, содержащем значительное количество соляной кислоты, также создает благоприятные условия для выделения родия. [18]
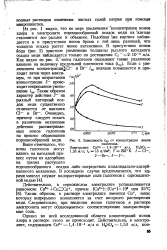 |
Зависимость inp от концентрации ионов. [19] |
Из рис. 1 видно, что по мере увеличения концентрации ионов хлора в электролите порошкообразный осадок меди на гкатоде становится все рыхлее и объемнее. Подобная рке картина наблюдается и в присутствии ионов брома с той лишь разницей, что толщина осадка растет менее интенсивно. Если с увеличением концентрации С1 - и Вг - inp вначале повышается и проходит затем через макси-мум, то при возрастании концентрации J - происходит непрерывное уменьшение tnp. Очевидно, причину следует искать в различном механизме действия рассматриваемых ионов галогенов на процесс образования порошкообразной меди. [20]
В присутствии иона Г слой бензола окрашивается в красно-фиолетовый цвет, даже если одновременно присутствует ион брома. Если иона Г в анализируемом растворе нет, в присутствии ионов брома слой бензола окрашивается в соломенно-желтый цвет. Если в анализируемом растворе нет ни 1 -, ни Вг -, слой бензола остается бесцветным. [21]
В присутствии иона 1 - слой бензола окрашивается в красно-фиолетовый цвет, даже если одновременно присутствует ион брома. Если иона 1 - в анализируемом растворе нет, в присутствии ионов брома слой бензола окрашивается в соломенно-желтый цвет. Если в анализируемом растворе нет ни 1 -, ни Вг -, слой бензола остается бесцветным. [22]
AgCl указывает, что в нерастворимом остатке содержался хлорид серебра. Через несколько минут отделите от осадка раствор и определите в нем присутствие ионов брома и иода. [23]
В отсутствие сероводорода картина несюлько меняется. В этом случае на первый план по своей значимости выступают такие факторы, как присутствие ионов брома, йода, нефти и степени минерализации. [24]
Надо отметить, что способность десенсибилизировать часто совмещается с обратной способностью, и напротив, сенсибилизаторы, повышающие чувствительность в какой-то части спектра, заметно снижают чувствительность в остальном диапазоне. Например, один из лучших сенсибилизаторов - фено-сафраин заметно сенсибилизирует в зеленой части спектра; присутствие иона брома в больших количествах усиливает десенсибилизирующие свойства красителя. Понижение концентрации ионов брома, напротив, сильно повышает оптическую сенсибилизацию. [25]
Количественное определение ионов иода, брома и хлора при их совместном присутствии путем осаждения галогенидов серебра затруднено вследствие почти одинаковой растворимости галогенидов серебра. Однако в аммиачном растворе иодид серебра может быть частично осажден в чистом состоянии без примесей бромида и тем более хлорида серебра. Это позволяет определять ионы иода в присутствии ионов брома и хлора методом изотопного разбавления. [26]
Если иодиды были обнаружены при помощи описанной выше реакции ( § 51 6), то продолжайте прибавлять хлорную воду и встряхивать раствор до полного исчезновения фиолетовой окраски. Появление коричнево-желтого окрашивания ССЦ выделившимся свободным бромом указывает на присутствие ионов брома. Рекомендуется проделать контрольный опыт, взяв вместо приготовленного раствора дестиллиро-ванную воду, так как хлор, растворяясь в СС1Ь сообщает ему бледножелтую окраску, которая может быть ошибочно принята за окраску брома. [27]
В тех случаях, когда реакция нитрозирования идет медленно, например при нитрозировании моноэтиланилина, можно значительно ускорить реакцию и одновременно сделать конец ее более четким, если прибавить бромид калия, служащий катализатором процесса нитрозирования. Однако прибавление КВг не всегда допустимо. Например, в случае определения вторичных аминов в присутствии большого количества третичных аминов присутствие ионов брома может привести к неправильным результатам, так как они способствуют замещению нитрозогруппой водорода в ароматическом ядре третичного амина. [28]
Метод заключается в титровании серебра в аммиачном растворе иодидом калия с вращающимся платиновым электродом при - 0 23 б ( нас. Этот метод основан на работе Лайтинена и др. 21, показавших возможность точного амперометрического определения иона иода в аммиачном растворе в присутствии ионов брома и хлора при титровании нитратом серебра. [29]
Легко окисляющиеся амины диазотируют в слабокислой среде ( нейтральное диазотирование) при добавлении солей цинка или меди. Ионы цинка или меди должны предохранять амин от окислительного действия азотистой кислоты и тем способствовать гладкому течению реакции диазотирования. В серной кислоте диазотирование протекает медленнее, чем в соляной. Скорость диазотирования сильно увеличивается в присутствии ионов брома. [30]
Страницы: 1 2 3