Присутствие - ион - водород
Cтраница 1
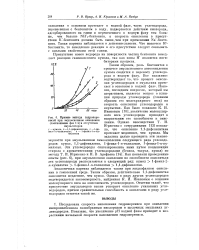 |
Кривые выхода гидроперекисей при эмульсионном окислении ( соотношение фаз в отсутствие эмульгаторов. [1] |
Присутствие ионов водорода на поверхности частиц бентонита замедляет реакцию самоокисления кумола, так как ионы Н являются ингибиторами процесса. [2]
В присутствии ионов водорода ( гидроксония Н8О) протофильным становится ацетон. [3]
В присутствии ионов водорода ( гидроксония Н3О) протофильным становится ацетон. [4]
В присутствии ионов водорода она снижается до 25 6 ккал / моль. Еще большее каталитическое действие оказывает фермент сахараза. В его присутствии энергия активации этой реакции составляет всего 9 4 ккал / моль. [5]
В присутствии ионов водорода она снижается до 25 6 ккал / моль. Еще большее каталитическое действие оказывает фермент сахара-за. В его присутствии энергия активации этой реакции составляет всего 9 4 ккал / моль. [6]
В присутствии ионов водорода некоторое количество бромид-ионов превращается в бромистый водород, так как в безводной среде отсутствует акцептор протонов. Таким образом, активность бромид-ионов уменьшается, а значение отношения окисленная форма - восстановленная форма увеличивается. При добавлении ацетата уменьшается концентрация ионов ацилония, увеличивается активность бромид-ионов и понижается окислительно-восстановительный потенциал. [7]
В присутствии ионов водорода кислоты и эфиры становятся значительно более энергичными ацилирующими средствами, но протекающие при этом каталитические реакции носят иной характер, идут по принципиально другому механизму ( стр. [8]
В присутствии ионов водорода кислоты и эфиры становятся значительно более энергичными ацилирующими средствами, о протекающие при этом каталитические реакции носят иной характер, идут по принципиально другому механизму ( стр. [9]
В кислой среде в присутствии ионов водорода ( гидроксония Н3О) протофильным становится ацетон. [10]
Так как кислотные свойства обусловлены присутствием ионов водорода в растворе, то значение концентрации ионов водорода соответствует активной кислотности. Недиссоциированная кислота в растворе составляет потенциальную кислотность. Сумма активной и потенциальной кислотности представляет собой общую кислотность. Общая кислотность определяется титрованием щелочью и называется титруемой или аналитической кислотностью. У всех кислот равной нормальности общая кислотность одинакова, соотношение же активной и потенциальной кислотностей будет определяться степенью диссоциации. [11]
 |
Модели молекулы муравьиной кислоты. [12] |
Поэтому скорость разложения муравьиной кислоты в присутствии ионов водорода значительно увеличивается. [13]
 |
Каталитическое действие кислот. [14] |
Многие реакции в растворах ускоряются в присутствии ионов водорода и гидроксила, например, этерификация кислот и спиртов, гидролиз сложных эфиров. [15]
Страницы: 1 2 3 4