Присутствие - свободный ион
Cтраница 1
Присутствие свободного иона Mg2 в эфирном растворе кажется маловероятным вследствие малой диэлектрической постоянной растворителя. Металлический магний, осаждающийся при электролизе эквимолекулярной смеси ( C2H5) 2Mg и Mg28Br2, нерадиоактивен. [1]
Присутствие свободных ионов в растворе по-разному влияет на спектр ЯМР растворителя. Электрическое поле, создаваемое ионами, приводит к возмущению распределения зарядов в соседних молекулах растворителя и в результате изменяет электронное экранирование их ядер. Это в свою очередь изменяет положение линий спектра ЯМР. [2]
Присутствие свободного иона Mg2 в эфирном растворе кажется маловероятным вследствие малой диэлектрической постоянной растворителя. Металлический магний, осаждающийся при электролизе эквимолекулярной смеси ( C2H5) 2Mg и Mg28Br2, нерадиоактивен. [3]
Синей окраски, указывающей на присутствие свободного иона двухвалентного железа, не должно быть. К 20 каплям 5 % - ного раствора красной кровяной соли добавляют каплю 5 % - ного раствора хлорного железа и каплю 10 % - ной соляной кислоты. Синей окраски, указывающей при этой реакции на примесь желтой кровяной соли, также не должно быть. Навеску 1 65 г красной кровяной соли, соответствующей перечисленным требованиям, растворяют в мерной колбе на 1 л и после того, как соль растворится, в колбу вносят 10 6 г прокаленного в муфеле или на горелке углекислого натрия, растворяют его и добавляют воду до метки. [4]
В некоторых системах нарушение структуры растворителя, связанное с присутствием свободных ионов, дает вклад в стабилизацию ионных пар. Этот фактор часто играет заметную роль п водных растворах, поскольку жидкая вода имеет вполне определенную и сравнительно устойчивую структуру. Недавно в работе Кэя и др. [23] обсуждался пример такого эффекта, который дает вклад в стабилизацию ионных пар в метаноле. [5]
Перед каждым определением после регенерации колонку про мывают дистиллированной водой и делают пробу с метилоранжем на присутствие свободных ионов водорода. [6]
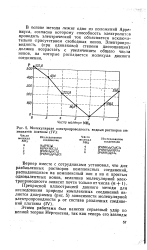 |
Молекулярная электропроводность водных растворов аммиакатов платины ( IV. [7] |
В основе метода лежит одно из положений Арре-ниуса, согласно которому способность электролитов проводить электрический ток объясняется исключительно Присутствием свободных ионов. [8]
Для определения эквивалентной точки при титровании ионов металлов с ЭДТА необходимо использовать подходящий индикатор, который будет реагировать на присутствие свободных ионов металлов в растворе. Таким индикатором, первоначально использованным Шварценбахом для титрования ионов кальция, был мурексид ( пурпурат аммония), который в настоящее время очень редко применяется. Этот индикатор имеет синюю окраску в аммиачном растворе, но дает красные комплексы со многими - ионами металлов в этом растворе. [9]
Следовательно, только при общей концентрации трилоната кальция, превышающей 1 мг-экв 1л, представляется возможным обнаружить особо чувствительными реактивами присутствие свободных ионов кальция в растворе. Столь же и даже более прочные комплексы образует трилон Б с катионами других металлов. В табл. 13 - 1 приведены величины К для некоторых катионов, обычно присутствующих в водах теплосилового хозяйства. Для удобства сравнения приведены десятичные логарифмы констант, взятые с обратным знаком. Таким образом, самые прочные комплексы из числа перечисленных образуют трехвалентные кобальт, железо и хром. Затем следуют никель, свинец, медь, цинк, алюминий и двухвалентный кобальт. [10]
Следовательно, только при общей концентрации трило-ната кальция, превышающей 1 мг-экв / л, представляется возможным обнаружить особо чувствительными реактивами присутствие свободных ионов кальция в растворе. Столь же и даже более прочные комплексы образует трилон Б с катионами других металлов. [11]
Из термодинамических соображений необходимость допущений такого равновесия вытекает с полной несомненностью, и можно предположить, что именно эти равновесия и определяют собой потенциал раствора. Но так как и присутствие свободных ионов в растворе принципиально вряд ли может быть оспариваемо, то возникает вопрос, кому в данном случае принадлежит руководящая роль, галогенам или свободным ионам. Для ответа на этот вопрос мы должны хотя бы приблизительно оценить равновесную концентрацию свободных галогенов в наших системах, что можно сделать на основании известных величин нормальных потенциалов галогенов с помощью уравнения Нернста. [12]
Большое значение для действия ядов на растение имеет степень электролитической диссоциации. Ожигающее действие препаратов обусловлено присутствием свободных ионов водорода. В связи с этим недопустимо наличие в пестицидных препаратах избыточного количества свободных минеральных кислот и кислых солей. [13]
Для этого применяют раствор хлорида железа ( 10 г РеС13 в. После отстаивания и отделения раствора от осадка в растворе должен находиться 0 1 - 0, 15 % - ный избыток С1 - - ионов Индикатором служит роданид аммония. В присутствии свободных ионов железа возникает красное окрашивание. [14]
После отстаивания и отделения раствора от осадка в растворе должен находиться 0 1 - 0 15 % - ный избыток С1 - - ионов. Индикатором служит роданид аммония. В присутствии свободных ионов железа возникает красное окрашивание. [15]
Страницы: 1 2