Присутствие - катализатор
Cтраница 2
Присутствие катализатора не нарушает также состава равновесных смесей, свойственных данным температурам. [16]
Присутствие катализатора и здесь играет решающую положительную роль. [17]
Присутствие катализаторов, применимых в жидкой фазе, способствует хлорированию в парах; в частности, хлорное железо содействует полихлорированию - увеличению содержания дихлорбензола и появлению трихлорбензолап. [18]
Присутствие катализатора снижает энергию активации реакций крекинга и благодаря этому скорость каталитического крекинга значительно выше, чем термического. Так, например, каталитический крекинг нафтенов протекает в 500 - 4000 раз быстрее, чем соответствующий термический. [19]
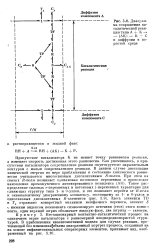 |
Диаграмма сопряжения каталитической реакции типа А К - - ( АК - К -. - С и диффузии в пористой среде. [20] |
Присутствие катализатора К не меняет точку равновесия реакции, а изменяет скорость достижения этого равновесия. Как упоминалось, в присутствии катализатора сопротивление реакции шунтируется параллельным контуром с малым сопротивлением реакции. В данном случае диссипация химической энергии по мере приближения к состоянию химического равновесия учитывается многосвязным диссипативным Я-полем. Здесь элементы TD и Тд отражают конкретный механизм межфазного переноса, элемент S с нижним индексом компонента символизирует источник ( сток) этого компонента, один верхний штрих обозначает жидкую фазу, два штриха - газовую. [21]
Присутствие катализаторов резко снижает - эндотермичность этих реакций. [22]
Присутствие катализатора не требуется, и реакции могут протекать через нуклеофильную атаку олефинов. [23]
Присутствие катализатора создает кроме необходимого полезного эффекта, ряд технологических трудностей. Главные из них - необходимость удаления катализатора из реакционной массы, возможность коррозии оборудования, опасность загрязнений окружающей среды продуктами, получающимися при нейтрализации катализатора. Иногда существенным может быть и потеря веществ, используемых в качестве катализатора. [24]
Присутствие катализатора в виде отдельной фазы ограничивает температуру проведения этой сильно экзотермической реакции-130 С, так как при более высоких температурах комплекс катализатора разрушается и быстро теряет активность. Кроме того, более высокие температуры благоприятствуют образованию He-ароматических и конденсированных ароматических веществ, которые являются основными и хорошо растворяются в кислом катализаторе. Однофазная реакционная система позволяет избежать этих нежелательных процессов и повысить температуру реакции до 140 - 200 С, что снижает издержки на отвод тепла. Гомогенность системы достигается путем тщательного контроля условий реакции и поддержания концентрации А1С13 в пределах растворимости. В настоящее время фирма Lummus проектирует завод, который будет использовать разбавленный поток этилена в качестве сырья. [25]
Присутствие катализатора дает реакции возможность протекать по новому механизму. Конечно, реакция может происходить так же и по старому механизму. Но уже сам факт, что в присутствии катализатора возможен новый, дополнительный механизм, означает, что суммарная реакция ускоряется. В действительности скорость реакции, идущей по новому механизму, обычно уже сама по себе значительно превосходит скорость реакции, идущей по старому механизму. Поэтому общая скорость реакции значительно возрастает. Хорошим катализатором считается такой, который вызывает наибольшее изменение скорости реакции. Катализатор может ускорять реакцию либо потому, что он облегчает ориентацию, либо потому, что новый механизм требует меньшей энергии активации, либо, наконец, по обеим причинам одновременно. Энергия активации каталитических реакций бывает и в самом деле низкой. При реакции окисления глюкозы, которую мы рассматривали во второй главе, катализатором служили метиленовая синь, ионы гидроксила и вода. [26]
 |
Изменение энергии в ходе каталитической реакции. [27] |
Присутствие катализатора вызывает зарождение цепных реакций, приводит к замене трудно осуществимых стадий с тройными столкновениями на более вероятные стадии с двойными столкновениями. [28]
Присутствие катализатора не может изменить положение точки эквивалентности, так как его назначение только в ускорении установления равновесия. [29]
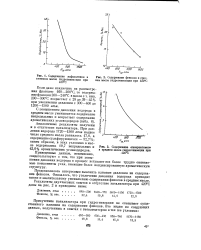 |
Содержание фенолов в среднем масле гидрогенизации при 420 С.| Содержание гетероатомов. [30] |
Страницы: 1 2 3 4