Присутствие - угольная кислота
Cтраница 2
В качестве материала для изготовления труб подогревателей рекомендуется применять нержавеющие стали, но яе латунь, которая в присутствии угольной кислоты подвергается обесцинкованию. [16]
Разница в значениях измеренной хп и расчетной кр удельных электрических проводимостей Ах в обессоленном конденсате и питательной воде может объясняться присутствием угольной кислоты и органических веществ, а также вымыванием продуктов разложения ионитов. Как показывает опыт эксплуатации отечественных конденсатоочисток при непрерывной их работе и скорости фильтрации около 50 м / ч, предположение о загрязнении обессоленного конденсата продуктами разложения ионитов не обосновано. В то же время наличие углекислоты и органики в обессоленном конденсате вполне реально. [17]
 |
Схема коррозийных микро-пар. [18] |
На интенсивность протекания электрохимической коррозии в воде и рассолах большое влияние оказывают наличие растворенного в них кислорода, водородный показатель рН, присутствие угольной кислоты. [19]
При титровании слабых кислот, какой является СН3СООН, в присутствии угольной кислоты, находящейся в их водных растворах и в дистиллированной воде, а также образующейся при нейтрализации карбонатов, содержащихся в растворах оснований, результаты анализа искажаются. [20]
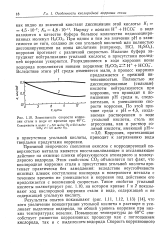 |
Зависимость скорости коррозии стали в воде от времени при 40 С. [21] |
Причиной непрочного сцепления окислов с корродирующей поверхностью металла является восстанавливающее и отслаивающее действие на окисные пленки образующегося атомарного и молекулярного водорода. Этим свойством СО2 объясняется тот факт, что кислородная коррозия стали в присутствии угольной кислоты протекает практически без замедления: вследствие неустойчивости окисных пленок поступление кислорода к поверхности металла с течением времени не уменьшается и коррозия под действием его продолжается с неизменной скоростью. Такое свойство угольной кислоты иллюстрирует рис. 1.10, на котором кривые / и 2 показывают ход кислородной коррозии стали в воде, содержащей и не содержащей угольную кислоту. [22]
Угольная кислота в процессе коррозии с кислородной и водородной деполяризацией не нейтрализуется, содержание ее остается почти неизменным, и кислородная коррозия стали не уменьшается со временем. Несмотря на то что коррозия с выделением водорода составляет всего лишь 2 5 - 4 % общей скорости разрушения, большинство случаев коррозии стального оборудования обусловлено ею, так как в присутствии угольной кислоты создаются условия, благоприятствующие протеканию кислородной коррозии. [23]
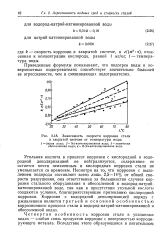 |
Зависимость скорости коррозии стали. [24] |
Угольная кислота в процессе коррозии с кислородной и водородной деполяризацией не нейтрализуется, содержание ее остается почти неизменным и кислородная коррозия стали не уменьшается со временем. Несмотря на то, что коррозия с выделением водорода составляет всего лишь 2 5 - 14 % от общей скорости разрушения, она ответственна за большинство случаев коррозии стального оборудования в обессоленной и водород-натрий-катионированной воде, так как в присутствии угольной кислоты создаются условия, благоприятствующие протеканию кислородной коррозии. Коррозия с водородной деполяризацией наряду с ржавлением является т р етье и и основной особенностью коррозионного процесса стали в водород-натрий-катионированной и обессоленной водах. [25]
Однако увеличение концентрации водородных ионов будет значительно ускорять растворение металла. В присутствии угольной кислоты образуется сначала гидрокарбонат двухвалентного железа Ре ( НСОз) г; когда двухвалентное железо окисляется до трехвалентного, угольная кислота освобождается, потому что карбонат трехвалентного железа не существует. Освобожденная кислота снова оказывает свое действие на металл, и скорость его ржавления значительно увеличивается. [26]
Однако увеличение концентрации водородных иоиов будет значительно ускорять растворение металла. В присутствии угольной кислоты образуется сначала гидрокарбонат двухвалентного железа Fe ( BCOs) z; когда двухвалентное железо окисляется до трехвалентного, угольная кислота освобождается, потому что карбонат трехвалентного железа не существует. Освобожденная кислота снова оказывает свое действие на металл, и скорость его ржавления значительно увеличивается. [27]
В эксплуатационных условиях кислородная коррозия стали, контактирующей с конденсатом, может усиливаться действием ряда факторов. Главными из них являются наличие уголь-яой кислоты, хлоридов, сульфатов, гидроксида и оксида железа, нагревание и действие тепловых нагрузок. В присутствии угольной кислоты наряду с протеканием коррозии с кислородной деполяризацией развивается коррозия с водородной деполяризацией. Выделяющийся при этом атомный водород частично восстанавливает оксидную защитную пленку. Образование молекулярного водорода приводит и к ее отслаиванию. В результате скорость кислородной коррозии стали в конденсате в присутствии угольной кислоты ( так же, как и в химически обработанных водах) практически не изменяется по времени. Среда обогащается оксидами железа, ухудшающими качество конденсата. [28]
Карбонат бария ВаСО3 устойчив при достаточно высоких температурах. Давление диссоциации при 1200 С равно 92 мм рт. ст., при 1400 оно составляет - 1 атм. Растворимость его повышается в присутствии угольной кислоты. [29]
 |
Индикаторы, применяемые для титрования различных кислот и оснований. [30] |
Страницы: 1 2 3