Присутствие - белок
Cтраница 2
Появление фиолетовой окраски указывает на присутствие белка. [16]
Правильность объемного определения хлоридов в присутствии белка, например, в случае прямого определения хлоридов в сыворотке крови, была проверена авторами сравнением результатов, полученных при прямом титровании, с результатами, полученными при определении хлоридов в таких же образцах, которые, однако, предварительно были подвергнуты озолению в платиновом тигле в присутствии избытка бикарбоната натрия. При этом не было обнаружено заметной разницы. Следует указать, что оголение в отсутствии бикарбоната натрия всегда приводило к заметным потерям хлорида. [17]
Появление коагулирующей красной массы указывает на присутствие белка. Неорганические соли мешают пробе, поскольку они осаждают ртуть из реактива. [18]
Показания стеклянного электрода не точны в присутствии белков и других органических соединений с большими молекулами, которые адсорбируются на его поверхности. Стеклянный электрод нельзя использовать в сильнощелочной среде, или в кислых растворах, содержащих F -, так как в этих условиях его поверхность разъедается. Так, при рН 10 в присутствии Na с концентрацией 1 г-ион / л отсчитанные значения на ОД-02 единицы рН ниже, а при рН 12 -примерно на единицу рН ниже. [19]
 |
Температура застывания и плавления некоторых жиров и масел. [20] |
В воде они нерастворимы; но в присутствии белка или щелочи образуют достаточно прочные эмульсии. Примером жировой эмульсии может служить молоко. Все жиры хорошо растворимы в бензине, эфире, сероуглероде, хлороформе, четырех-хлористом углероде; в спирте растворимость для многих жиров меньше. [21]
В воде они нерастворимы; но в присутствии белка или щелочи образуют достаточно прочные эмульсии. Примером жировой эмульсии может служить молоко. Все жиры хорошо растворимы в бензине, эфире, сероуглероде, хлороформе, четыреххлори-стом углероде; в спирте растворимость для многих жиров меньше. [22]
Бдедножелтое, переходящее в оранжевое окрашивание указывает на присутствие белков, желтое, переходящее в темнокоричневое окрашивание, указывает на присутствие сульфонамидов. [23]
Элюат ( фракции по 20 мл) анализируют на присутствие белка на спектрофотометре при 280 нм. Конканавалин А элюируют 0 10 М раствором D-ГЛЮКОЗЫ в 1 0 М растворе хлористого натрия. Фракции с оптической плотностью не ниже 0 10 собирают и диализуют против большого объема 1 0 М раствора хлористого натрия, причем последний несколько раз меняют. [24]
Попова [2] наблюдали усиление связывания основных красителей РНК в присутствии белка. [25]
В мерные пробирки собирают по 1 мл элюата и проверяют присутствие белка по биуретовой реакции. Для этого к каждой фракции добавляют 0 1 мл 4 - % - ного раствора CuS04 и 1 мл 10 % - ного раствора NaOH. При наличии белка раствор окрашивается в фиолетовый цвет. Как только в 2 - 3 последних фракциях реакция иа белок будет отрицательной, раствор из колонки выпускают, оставив над целлюлозой 0 5 см жидкости, и начинают элюирование 1 М NaCl. Также собирают фракции по 1 мл и проводят качественную реакцию на белок. [26]
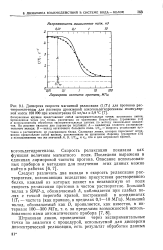 |
Дисперсия скорости магнитной релаксации ( l / 7 i для протонов растворителя-воды для раствора дрожжевой алкогольдегидрогеназы молекулярной массы 160000 при концентрации 65 мг / мл и 5 9 С. [27] |
Следует различать два вклада в скорость релаксации растворителя, возникающих вследствие присутствия растворенного белка, каждый из которых влияет на независимую от поля скорость релаксации протонов в чистом растворителе. [28]
Одинцов и Сергеева [108] нашли значительное количество азота, что указывало на присутствие белка в лигнине, выделенном из тканей живого растения крепкими минеральными кислотами. Поэтому они сделали вывод, что эти методы непригодны для определения содержания лигнина в таких материалах, как еловые почки и листья хлопка. [29]
В холостом опыте образуется желтая окраска, в то время как в присутствии белка раствор окрашивается в глубокий синий цвет. [30]
Страницы: 1 2 3 4