Присутствие - нитрат-ион
Cтраница 2
Остальные условия проведения реакции те же, что и при обнаружении МОз-ионов - Реакция применима для обнаружения нитрит-ионов в присутствии нитрат-ионов, если проводить ее в слабокислой среде. [16]
При комнатной температуре между этими комплексами быстро устанавливается равновесие. Присутствие нитрат-иона способствует образованию высших нитратных комплексов. [17]
Си растворяют в 5 мл HNO3 ( 1: 1) при нагревании, раз - 0 6355 СиП бавляют водой до 50 мл, кипятят до удаления оксидов азота, до - ( 10-а М) водят водой до 1 л в мерной колбе. Если присутствие нитрат-ионов мешает, то после растворения трижды выпаривают с 5 мл конц. Си растворяют в 10 мл HNO3 ( 1: 1), приливают 1 мл конц. [18]
КЗ каплям испытуемого раствора добавляют 9 капель концентрированной H2SO4 и 3 капли раствора бруцина, все перемешивают стеклянной палочкой. В присутствии нитрат-иона появляется ярко-розовое окрашивание, переходящее в золотистое. Если присутствует нитрит-ион, то его разрушают одним из способов, описанных в § 116, и открывают нитрат-ион. Для этого к 5 каплям раствора добавляют 5 капель 30 % - ного раствора щелочи и несколько кусочков металлического цинка или сплава Деварда. Оставляют стоять на холоду 20 мин. Открытый конец полумикропробирки накрывают фильтровальной бумажкой, смоченной реактивом Нес-слера. Выделяющийся аммиак образует красно-коричневое пятно. [19]
К капле нейтрального или уксуснокислого исследуемого раствора объемом 0 03 мл прибавляют на капельной пластинке по капле раствора сульфаниловой кислоты и раствора сс-нафтиламина и несколько крупинок цинковой пыли. В присутствии нитрат-иона постепенно появляется розовое окрашивание, обусловленное образованием азокрасителя. [20]
Важным моментом, отражающимся на точности определения, является предохранение первоначально полученной кремниевой кислоты от образования полимерных форм и выделения ее в нерастворимой форме. Эти процессы затруднены в присутствии нитрат-ионов, поэтому пробу следует растворять в азотной кислоте, нагретой примерно до 80 - 90 С. Нагревание до более высокой температуры нежелательно, поскольку приводит к получению нерастворимой кремниевой кислоты и соответственно к заниженным результатам для кремния. [21]
По данным работы [16, 17] эффективность блескообразующих добавок зависит от строения молекул поверхностно-активных веществ и определяется расстоянием между атомами серы и углерода в молекуле ПАВ. Эффективность большинства блескообразующих добавок снижается в присутствии нитрат-ионов и при увеличении температуры электролита. [23]
Это означает, что если реакция проводится в присутствии нук-леофилов, то на второй стадии будет наблюдаться конкуренция их с бромидом, освободившимся из молекулы брома. Аналогичные результаты получены при проведении реакции в присутствии нитрат-ионов и воды. [24]
Внесите в раствор несколько кусочков ( стружек) металлического алюминия и закройте отверстие пробирки полоской красной лакмусовой бумаги. Посинение бумаги ( вследствие выделения аммиака) указывает на присутствие нитрат-ионов. [25]
Поместите 2 капли раствора дифениламина в коническую пробирку и прилейте осторожно по стенке 2 капли приготовленного раствора, предварительно подкисленного серной кислотой. Появление синего кольца на поверхности соприкосновения двух растворов указывает на присутствие нитрат-ионов. Эта реакция неприменима в присутствии других окислителей. [26]
В пробирку помещают 1 - 2 небольших кристалла FeSO4, добавляют 2 - 3 капли испытуемого раствора, а затем во избежание перемешивания осторожно, по стенке пробирки, добавляют одну каплю концентрированной серной кислоты. Образование бурого кольца на границе двух слоев жидкости свидетельствует о присутствии нитрат-ионов. [27]
В пробирку помещают 1 - 2 небольших кристалла FeSO - t, добавляют 2 - 3 капли испытуемого раствора, а затем во избежание перемешивания осторожно, по стенке пробирки, добавляют одну каплю концентрированной серной кислоты. Образование бурого кольца на границе двух слоев жидкости свидетельствует о присутствии нитрат-ионов. [28]
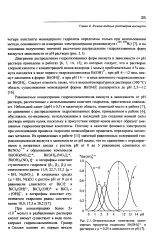 |
Относительные количества мономерных продуктов гидролиза Bi ( OH в растворах с ц 0 25 в зависимости от рН. [29] |
Равновесные концентрации гидроксокомплексов висмута в зависимости от рН раствора, рассчитанные с использованием констант гидролиза, практически совпадают. Небольшой сдвиг ( АрН s 0 3) в щелочную область, имеющий место в работе [7], по сравнению с распределением гидролизованных форм, приведенным в работе [6], обусловлен, по-видимому, использованием в последней для создания ионной силы раствора нитрата калия, поскольку в присутствии нитрат-ионов висмут образует смешанные гидроксонитратные комплексы. Поэтому в качестве фонового электролита при исследовании процесса гидролиза целесообразно применять перхлораты щелочных металлов. [30]
Страницы: 1 2 3 4
