Присутствие - окись - азот
Cтраница 2
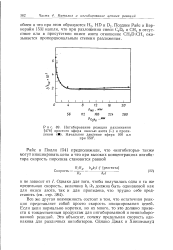 |
Ингибирование реакции разложения простого эфира окисью азота ( О и пропиленом (. Начальное давление эфира 100 мм при 550. [16] |
Позднее Раис и Вэр-нерайн [53] нашли, что при разложении смеси C2D6 и СН4 в отсутствие или в присутствии окиси азота отношение CH3D / CH4 оказывается пропорциональным степени разложения. [17]
Порядок увеличения окисления для различного пламени имеет тот же характер, что и для возрастания содержания атомного кислорода в пламени, установленный Гэйдоном в присутствии окиси азота. [18]
Для объяснения образования дисилокеана и азота, а также повышенной скорости образования водорода в реакции фотосинтеза метилсиланов CHsSiHa, ( CHabSif - b, ( СН3) з5Ш в присутствии окиси азота высказано. [19]
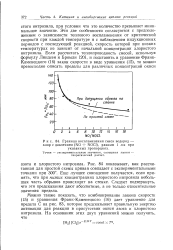 |
Граница воспламенения смеси водород. [20] |
Можно также показать, что комбинирование закона скорости ( 15) и уравнения Франк-Каменецкого ( 16) дает уравнение для предела С на рис. 83, которое предсказывает правильную энергию активации для реакции в присутствии окиси азота и хлористого нитрозила. [21]
Это последнее свойство пятихлористой сурьмы заставляет применять ее во многих случаях для передачи хлора, тем более, что отделивши хлор, она оставляет SbQ3, которая вновь может поглощать хлор, и потому многие вещества, не способные прямо реагировать с газообразным хлором, реагируют с пятихлористою сурьмою, и в присутствии небольшого ее количества хлор на них действует, подобно тому, как в присутствии окиси азота кислород способен окислять и такие тела, которые сами не могут окисляться на счет свободного кислорода. Трех - и пятихлористая сурьма, имея хлорангидрид-ный характер, дымят на воздухе, притягивают влагу и водою разлагаются, обра-вуя при втом сурьмянистую и сурьмяную кислоты. Но треххлористая сурьма при первом действии воды не выделяет всего хлора в виде хлористого водорода, что и понятно из того, что сурьмянистый ангидрид в то же время есть основание, а потому может реагировать с кислотами; и действительно, даже сернистая сурьма, растворенная в избытке крепкой соляной кислоты ( причем развивается H - S), дает водный раствор треххлористой сурьмы, который при осторожной перегонке дает даже безводную треххлорнстую сурьму. Первое действие воды состоит в образовании хлорокисн SbOCl, но состав продукта изменчив, смотря по относительному количеству воды, а именно, оно меняется между пределами SbOCI и ЗЬЮ С. Сурьма образует с бромом и иодом такие же соединения, как и с хлором; SbBr3 кристаллизуется в бесцветных призмах, плавится при 94 и кипит при 270, a SbJ3 представляет красные кристаллы, уд. Последняя дает легко растворимые двойные соли с фтористыми щелочными металлами. Дитт и Метцнер ( 1892) показали, что Sb и Bl растворяются в соляной кислоте только от участия в реакции кислорода воздуха или растворенного в кислоте. [22]
Исследовано влияние окиси азота на степень окисления аммиака на железохромовом катализаторе. Присутствие окиси азота в аммиачно-воздушной смеси снижает степень окисления аммиака. Однако при температуре, определяемой уравнением ( 1), степень окисления аммиака в чистой аммиачно-воздушной смеси и в газовой смеси с примесью окиси азота одинакова. [23]
Окислы азота могут попадать с воздухом в ВРУ, расположенные вблизи производств азотной кислоты. В присутствии окиси азота ускоряется процесс полимеризации ненасыщенных углеводородов и особенно бутадиена и циклопентадиена. Физико-химические процессы взаимодействия окислов азота с органическими продуктами, которые могут накапливаться в аппаратуре ВРУ в условиях низких температур, еще недостаточно изучены. Однако случаи взрывов концентрированных углеводородных смесей с окислами азота в аппаратуре низкотемпературной промывки промышленных газов и ВРУ дают основания считать окислы азота весьма опасными примесями в воздухе, поступающем на разделение. Такая опасность усиливается при повышении температуры во время отогрева и последующих пусках ВРУ. [24]
Между влиянием окиси азота и галоидсодержащих соединений, однако, имеется существенное различие. В присутствии окиси азота состав продуктов разложения ацетилена не меняется, а при введении галоидсодержащих соединений ( особенно бромистого зтила) образование бензола и полимеров ацетилена почти полностью прекращается и в основном появляются этилен и метан. [25]
Так как окись азота не оказывает влияния на скорость реакции, автор пришея к выводу, что отщепление воды протекает мономолекулярно. Однако значительное снижение скорости в присутствии окиси азота может соответствовать одному или другому либо обоим указанным выше процессам. [26]
Так как окись азота не оказывает влияния на скорость реакции, автор пришел к выводу, что отщепление воды протекает мономолекулярно. Однако значительное снижение скорости в присутствии окиси азота может соответствовать одному или другому либо обоим указанным выше процессам. [27]
Стици и Фолкинс [43], Клут и Вальтере [24] исследовали влиярие окиси азота на термическое разложение, сенсибилизированное соединениями, легко расщепляющимися на свободные радикалы. Их работами было показано, что в присутствии окиси азота должна иметь место некоторая остаточная цепная реакция. [28]
Технологический режим процесса синтеза концентрированной азотной кислоты должен обеспечить высокую степень превращения компонентов реакции и ее большую скорость. Поскольку скорость образования азотной кислоты сильно тормозится в присутствии окиси азота, следует прежде всего максимально ускорить окисление NO. Это вызывает необходимость создания высокого парциального давления кислорода и проведения процесса под давлением до 40 ат. В связи с высоким давлением процесса синтеза концентрированной азотной кислоты требуется ведение его при повышенной температуре. При низких температурах реакция ( 4) разложения азотистой кислоты или реакция ( 5) ее окисления лимитируют общую скорость процесса. С повышением температуры увеличивается количество четырехокиси азота, превращающейся в МОг, и возрастает скорость гидролиза двуокиси азота водой. Кроме того, как для смещения равновесия, так и для увеличения скорости реакции необходим значительный избыток четырехокиси азота по сравнению с ее теоретическим количеством. В этих условиях возможен синтез 98 - 99 % - ной азотной кислоты с относительно большой скоростью. [29]
В пользу механизма свободных радикалов имеются весьма убедительные доказательства. Тем не менее, наличие остаточной скорости реакции в присутствии окиси азота указывает на то, что имеет место и молекулярны и механизм. По-видимому, следует признать действие обоих механизмов. Тот факт, что средняя длина цепи гораздо короче, чем предполагаемая, указывает на наличие небольшого числа цепей, но достаточной длины. [30]
Страницы: 1 2 3