Присутствие - окись - азот
Cтраница 3
Ни одно из этих заключений не является экспериментально доказанным. С целью выяснения вопроса о природе промежуточных стадий реакции ( 1) нами было изучено взаимодействие магний-бромэтила с хлористым кобальтом и с трех - и четыреххлори-стым титаном в присутствии окиси азота, стирола иа-метилсти-рола. Все эти соединения количественно улавливают свободные радикалы, благодаря чему изучение их влияния на выход и соотношение между этаном и этиленом представляет собой прямой путь для установления свободнорадикальных стадий. В случае возникновения в ходе реакции свободных радикалов C2Hs - присутствие акцепторов свободных радикалов должно было бы полностью исключить образование этана и этилена. Показано, однако, что при проведении реакции между магний-бромэтилом и хлористым кобальтом при температуре от - 20 до 40 окись азота, стирол и а-метилстирол не вызывают уменьшения выхода этана и этилена и не влияют на соотношение между ними. [31]
В случае радикального механизма взаимодействие свободных радикалов цепи с D2 должно приводить к образованию продуктов, содержащих дейтерий. Молекулярный же распад са м по себе не может приводить к образованию обмененных продуктов. Было найдено, что как в присутствии окиси азота в количестве, достаточном для предельного торможения, так и без нее обмен всегда имел место. При этом оказалось, что при одинаковых глубинах превращения в обоих случаях ( с NO и без нее) в этилене наблюдается одинаковый обмен. Этот результат показывает, что предельно заторможенная реакция также является цепной, а не молекулярной. Этот опыт свободен от возражений о том, что дейтерированные вещества образуются в обоих случаях в результате независимых от реакции крекинга процессов обмена, например в результате поверхностных реакций, поскольку независимый процесс должен быть связан не с глубиной превращения, а только со временем. [32]
Реакции, идущие по радикальному механизму, по-видимому, более подвержены влиянию примесей веществ, которые могут инициировать или обрывать цепи, чем молекулярные процессы. Однако следует подчеркнуть, что окончательные выводы не могут быть полупены только из наблюдений скорости в присутствии таких веществ, как кислород, окись азота и пропилен. В частности, исследования торможения, проведенные в присутствии окиси азота, в последние годы были предметом многочисленных дискуссий, и их интерпретация, несомненно, намного сложнее, чем это было предложено первоначально. Исходя только из факта, что окись азота может действительно инициировать цепные реакции при соответствующих условиях [9], нет оснований предполагать, что остаточная реакция, идущая в присутствии избытка ингибитора, является мономолекулярной реакцией. [33]
Добавки двуокиси при 300 - 450 С и давлении 300 мм рт. ст. сокращают период индукции окисления и не влияют на выходы и химический состав продуктов реакции. Авторы считают, что сокращение периода индукции связано с. Изучая тот же процесс, но в несколько иных условиях, в присутствии окиси азота, Бейдер [88] нашел, что последняя уско-ряет все стадии окисления, смещает реакцию в области более, низких температур и увеличивает выход формальдегида. [34]
Фотохимический туман возникает в загрязненном воздухе в результате фотохимических реакций, протекающих под действием солнечного излучения. В ясные дни солнечная радиация вызывает расщепление молекул двуокиси азота с образованием окиси азота и атомарного кислорода. Атомарный кислород с молекулярным кислородом дает озон. Казалось бы, озон в присутствии окиси азота, окисляя последнюю, должен снова превратиться в молекулярный кислород, а окись азота - в двуокись. [35]
Пиролиз этана в реакторах обычного типа изучался весьма широко. Этот анализ приводит к выводу, что реакция протекает по механизму свободных радикалов и имеет кинетически первый порядок; энергия акти-вапии ее равна около 74 ккал / моль. Скорость в предположении кажущегося первого порядка реакции уменьшается при высоких степенях превращения. Обнаружено, что реакция в сильной степени тормозится присутствием окиси азота. Этилен и водород образуются примерно в одинаковых молярных количествах, наряду с ними получается лишь небольшое количество ( 2 - 5 % от количества этилена) метана и следы высококипящей жидкости. [36]
Гейдон применял этот метод как чисто качественный. Свечение служило индикатором на атомарный кислород. В работе Карми-ловой и Кондратьева [78], в которой были проведены измерения абсолютной интенсивности желто-зеленого свечения N02, показано, что интенсивность свечения количественно характеризует концентрацию атомарного кислорода в пламени СО. Позднее Джеймс и Сагден [79] показали, что интенсивность свечения продуктов сгорания водорода в присутствии окиси азота пропорциональна [ NO ] и концентрации атомов О, которая вычислялась по значениям констант равновесия. [37]
Согласно Грабаку [91], реакция перекиси бензоила с диметиланилином в растворе бензола характеризуется порядком 3 / 2 по отношению к каждому из компонентов. В растворе стирола или четыреххлористого углерода порядок реакции снижается до первого относительно каждого компонента. На этом основании Грабак считает, что реакция перекиси бензоила с диметиланилином в растворе бензола является цепной. Уменьшение в несколько раз скорости расхода перекиси бензоила в реакции с диметиланилином в растворе бензола в присутствии окиси азота также рассматривается как доказательство протекания цепной реакции. [38]
Согласно Грабаку [91], реакция перекиси бензоила с диметиланилином в растворе бензола характеризуется порядком 3 / 2 по отношению к каждому из компонентов. На этом основании Грабак считает, что реакция перекиси бензоила с диметиланилином в растворе бензола является цепной. Уменьшение в несколько раз скорости расхода перекиси бензоила в реакции с диметиланилином в растворе бензола в присутствии окиси азота также рассматривается как доказательство протекания цепной реакции. [39]
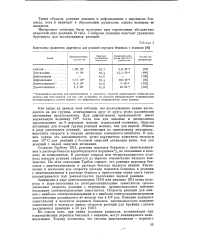 |
Константы уравнения Аррениуса для реакций перекиси бензоила с аминами. [40] |
Согласно Грабаку [92], реакция перекиси бензоила с диметиланили-ном в растворе бензола характеризуется порядком 3 / 2 по отношению к каждому из компонентов. В растворе стирола или четыреххлористого углерода порядок реакции снижается до первого относительно каждого компонента. На этом основании Грабак считает, что реакция перекиси бензоила с диметиланилином в растворе бензола является цепной. Уменьшение в несколько раз скорости расхода перекиси бензоила в реакции с диметиланилином в растворе бензола в присутствии окиси азота также рассматривается как доказательство протекания цепной реакции. [41]
Окисление дисульфидов в моно - и дисульфоксиды обычно идет с плохими выходами и для идентификации этих соединений не применяется. Строение фенилбутилсульфоксида не доказано, и вопрос о том, какой из двух атомов серы окислился, остается открытым. Моносульфоксид дибензилдисульфида неустойчив и при стоянии разлагается. Электролиз дифенилдисульфида приводит к бензосульфоновой кислоте ( выход 95 %) [27]; соответствующие сульфоновые кислоты получены при окислении диэтилдисульфида гипохлоритом [38] и диизобутилдисульфида кислородом в присутствии окиси азота. [42]
Одним из методов определения окиси азота является поглощение ее раствором едкого кали или едкого натра при пропускании воздуха. В результате реакции образуется азотистокислая соль, количество которой определяется колориметрически с помощью специального реактива путем сравнения со стандартными растворами азотисто-кислой соли. Этот реактив приготовляют следующим образом. Затем оба раствора смешивают и держат в хорошо закупоренной склянке. Анализируемый раствор едкой щелочи должен нейтрализоваться уксусной кислотой и иметь слабо кислую реакцию. В присутствии окиси азота указанный реактив дает оранжевое окрашивание. [43]
Страницы: 1 2 3