Присутствие - противоион
Cтраница 1
Присутствие противоионов в активированном комплексе компенсирует определенную часть электростатической составляющей в свободной энергии активации. [1]
Присутствие противоиона вблизи иона-реагента приводит также во многих случаях к кардинальным изменениям в реакционной способности и механизме реакции. Особенностью реакционных систем, способных существовать в растворе в виде равновесной смеси ионных частиц различного типа, является то, что каждая частица реагирует со своей собственной константой скорости и иногда дает свой собственный продукт. [2]
Так, в присутствии противоиона реакционная способность иона-реагента может снизиться на несколько порядков. В отдельных случаях ионные пары вообще не реагируют, тогда как свободные ионы образуют продукт со значительной скоростью. Кроме того, свободные ионы и ионные пары в реакции с одним и тем же реагентом могут давать различные продукты. Особенно часто ионная ассоциация меняет стереохимическую направленность процесса. [3]
Для каждой бинарной дисперсной системы в присутствии указанных противоионов на графике зависимости концентрация противоиона - рН имеется область, в которой оба золя остаются устойчивыми; устойчив также золь чистой кремневой кислоты, а латекс ПВХ коагулирует. Это наблюдение подтверждает, что кремневая кислота стабилизирует латекс ПВХ. [4]
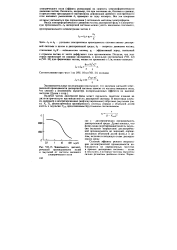 |
Зависимость диэлектрической проницаемости золей и эмульсий от частоты внешнего электрического поля. [5] |
Оказалось, например, что при значениях гвг, близких к единице, в присутствии трехзарядного противоиона деформация двойного электрического слоя вызывает уменьшение k примерно на одну четверть. [6]
Раствор, пропитывающий ионообменную мембрану, имеет большую, чем в диафрагме концентрацию ионов и электрический заряд, обусловленный присутствием противоионов мембраны. Благодаря наличию в пропитывающем мембрану растворе избытка ионов определенного знака ионообменная мембрана в электрическом поле пропускает ионы преимущественно этого знака, что позволяет использовать ее в процессах электролиза при получении продуктов повышенной чистоты. [7]
Увеличение степени гидролиза ПАА в растворах минерализованной воды приводит к еще большему агрегированию макромолекул, так как увеличение ионизации полииона в присутствии поливалентных противоионов создает предпосылки к дополнительной сшивке за счет образования межмолекулярных мостиков через поливалентные катионы. Даже при концентрации 0 0001 % ПАА в растворе дистиллированной воды и СаС12 наблюдались агрегаты размером в несколько микрон и множество агрегатов размером 60 - 100 нм, состоящих из нескольких отдельных глобул. Размер индивидуальных молекул не превышает 20 нм. Видны также крупные образования размером более микрона. Макромолекул, не участвующих в образовании агрегатов, встречается очень мало. [8]
Константы скорости роста свободного катиона и свободного аниона являются величинами более высокого порядка, чем константы скорости роста свободного радикала или иона в присутствии противоиона. Значительно меньшие величины констант скорости при росте свободных радикалов обусловлены высокой энергией активации. [9]
Под действием постоянного тока зоны белков располагаются непосредственно друг за другом, как бы складываются в стопку. В присутствии противоионов такие стопки из зон белка, имеющих различные значения рН, образуются между ведущими и замыкающими ионами. Скорость, с которой перемещаются зоны белка, и распределение концентраций ионов между их границами определяются концентрацией ведущих ионов. [10]
Наоборот, катионы вещества-основы, например Na, в отдельных случаях благоприятствуют экстракции анионных внутрикомплексных соединений. В присутствии подходящих противоионов, поставщиком которых служит соль макрокомпонента, полярными растворителями могут извлекаться заряженные формы хелато-образующего реагента, что вызовет сдвиг экстракционных равновесий. [11]
Область максимума различна для гидролизующихся солей алюминия и железа. В присутствии хлоридных противоионов она охватывает очень узкий интервал концентраций добавляемых солей, особенно в случае гидроокиси железа, что вполне согласуется с наблюдаемыми при очистке воды явлениями образования стабильных структур ( см. стр. В системе, образованной сульфатом алюминия, эта область растянута до точки эквивалентности раствора гидролизующейся соли и щелочного раствора, что характеризует более плотную упаковку сверхмицеллярных агрегатов в коагулятах гидроокиси алюминия, имеющей в качестве противоионов сульфатные ионы. [12]
В этом же ряду увеличивается скорость реакций обрыва цепи на противоионе. Так, в присутствии противоиона BFT ( BF3OR -) полимеризация тетрагидрофурана протекает практически без обрыва цепей [6, 17] с образованием живущих полимеров, при полимеризации же oc - окисей имеет место довольно интенсивный обрыв растущих цепей на противоионе [32, 54, 55], и реакция заканчивается до израсходования мономера в системе. Реакционная способность триалкилоксониевых а-окисных ионов столь велика, что они проявляют уже некоторые свойства, характерные для карбониевых ионов. Способность к сополимеризации а-окисей со стиролом падает в следующем ряду [56]: окись изобутилена окись пропилена окись стирола эпихлоргидрин. Очевидно, что в указанном ряду должен уменьшаться частичный положительный заряд на а-углеродном атоме окисного кольца вследствие уменьшения электродонорной способности заместителей. Эти результаты можно было бы интерпретировать и с точки зрения образования истинных карбониевых ионов в качестве активных частиц в этих системах, однако это предположение противоречит всем имеющимся данным, свидетельствующим, что и в случае а-окисей активные растущие центры представляют собой высокореакционноспособные триалкилоксониевые ионы. [13]
Ассоциация ионов влияет на их химическое поведение несколькими путями. Изменение плотности заряда и его распределение в ионе вследствие присутствия противоиона могут изменить реакционную способность иона. [14]
В таком кратком обзоре невозможно рассмотреть все вопросы, связанные с участием ионов и ионных пар, а также ассоциатов ионных пар в органических реакциях. Поэтому мы в первую очередь старались подчеркнуть наиболее характерные моменты, связанные с присутствием противоиона вблизи иона-реагента. В целом роль противоиона может быть и пассивной, и активной. В первом случае он снижает нуклеофильность ( или электрофильность) реагента, вследствие электростатического взаимодействия фрагментов ионной пары, или мешает по стерическим причинам реализовать определенные направления атаки. Во втором случае противоион за счет координации с каким-либо фрагментом второго реагента помогает своему противоположно заряженному партнеру или же направляет реакцию по определенному руслу. Знание этих сторон поведения противоиона совершенно необходимо химику-органику, решающему проблемы синтеза органических соединений и использующему для этих целей реагенты, способные существовать в растворе в виде ионных частиц различного типа. [15]
Страницы: 1 2