Присутствие - хлорид-ион
Cтраница 1
Присутствие хлорид-ионов приводит также к изменению характера коррозии: она становится более неравномерной, на поверхности металла появляются язвы, питтинги и сквозные свищи. [2]
Присутствие водорастворимого хлорид-иона в более чем следовых количествах обычно характерно для пород, содержащих галит, калсилит, карналит или другой эвапоритный минерал. Для определения водорастворимого хлорид-иона нагревают соответствующую навеску породы примерно со 100 мл воды до кипения. Кипятят 30 мин, фильтруют через плотный фильтр и промывают остаток теплой водой. Добавляют к фильтрату 5 мл концентрированной азотной кислоты и осаждают хлорид-ион раствором нитрата серебра, как описано ниже для кислоторастворимого хлора. [3]
Если присутствие хлорид-ионов и растворе нежелательно, используют ртутно-сульфатный электрод ( Hg / Hg2SO4 ( нас. В щелочном растворе применяют ртутно-оксидный электрод ( L 0 098 В отн. [4]
Например, присутствие хлорид-ионов заметно ослабляет окраску растворов роданида железа. Это связано с тем, что хлсрид-ионы образуют с железом ( III) бесцветный комплекс, который только в 40 раз менее прочен, чем роданидный-комплекс. [5]
Если титрование проводят в присутствии хлорид-ионов, то платина не мешает, так как хлорокомплексы платины ( II) и ( IV) достаточно прочны, чтобы помешать образованию комплекса с ЭДТА. Определению мешает Rh, в присутствии которого получаются заниженные по содержанию Pd результаты даже до 50 % О); о причине такого странного мешающего влияния ничего не известно. Если титрование осуществляют при комнатной температуре и быстро, то полученные в присутствии Ru и 1г заниженные результаты находятся в допустимых границах. Если Ru и Ir присутствуют в количестве 30 % ( вес. [6]
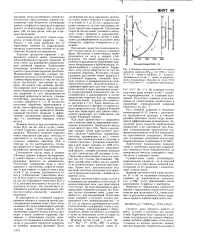
Таким образом, в присутствии хлорид-ионов скорости процессов ионизации и разряда индия увеличиваются. Из сдвига потенциала полуволны в отрицательную сторону с увеличением концентрации аниона ими был найден состав преобладающих комплексов индия в растворе, зарядность которых они подтвердили ионофоретическими исследованиями. [7]
Особенно полно проходив гидролиз в присутствии хлорид-ионов, когда выпадает в осадон очень мало растворимый хлороксид висмута BiOCl. Все это яв ляется причиной того, что в жидкой фазе сточных вод можно ожидать присутствия заметных количеств висмута только в том случае, если эти воды содержат свободную азотную кислоту в достаточно высокой концентрации. [8]
Наконец, бромид-ионы можно определить в присутствии хлорид-ионов, одним из описанных выше методов. [9]
Ионы олова восстанавливаются до металла в присутствии хлорид-ионов при потенциалах более отрицательных, чем - 0 6 в. Максимум тока электрохимического растворения металла не зависит от потенциала электрода в катодном цикле в интервале ( - 1 0) - ( - 1 2) в. Потенциал максимума анодной поляризационной кривой близок к - 0 5 в при окислении олова на фоне 1 М раствора хлорида аммония. [10]
Наконец, бромид-ионы можно определить в присутствии хлорид-ионов одним из описанных выше методов. [11]
Для определения фтора рекомендовались также соли свинца в присутствии хлорид-ионов: в таких условиях выпадает малорастворимый осадок8 - 10 PbClF. Талипов и Хадеев8 разработали и описали следующую методику определения фторидов. [12]
Для определения фтора рекомендовались также соли свинца в присутствии хлорид-ионов: в таких условиях выпадает малорастворимый осадок 8 - 10 PbClF. Талипов и Хадеев8 разработали и описали следующую методику определения фторидов. [13]
Выделение белого осадка AgCl или помутнение раствора указывают на присутствие хлорид-ионов в исходном анализируемом растворе. [14]
Соединение А быстро рацемизуется при нагревании до 100, однако присутствие хлорид-ионов не влияет на скорость процесса ни в хлороформе, ни в уксусной кислоте. Рацемизация, проводимая в дейтероуксусной кислоте ( CH3C02D), дает рацемическое соединение А, совершенно не содержащее дейтерия. [15]
Страницы: 1 2 3