Присутствие - электролит
Cтраница 1
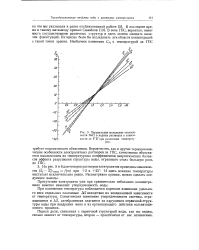 |
Парциальные Модальные теплоемкости NaCl в водных растворах в зависимости от Vт при различных температурах. [1] |
Присутствие электролита уже при сравнительно небольших концентрациях заметно изменяет упорядоченность воды. [2]
Присутствие электролитов особенно заметно сказывается на эффективности флотации коллоидных частиц. Вызывая уменьшение электрокинетического потенциала коллоидных примесей, они способствуют коагуляции и укрупнению частиц, что сопровождается ускорением процесса флотации. [3]
Присутствие электролита дает возможность проходить большим ионным токам и, следовательно, способствует коррозии. [4]
Присутствие электролитов изменяет скорость реакций, катализируемых кислотами и основаниями. Изложенное выше не оставляет сомнения в том, что реакции изотопного обмена водорода находятся в общем ряду с другими реакциями, протекающими при катализе кислотами и основаниями. Это справедливо также в отношении кинетического солевого эффекта при водородном обмене. Правда, солевой эффект при водородном обмене пока изучен очень мало. [5]
Присутствие электролита дает возможность проходить большим ионным токам и, следовательно, способствует коррозии. [6]
Присутствие электролитов ( неорганических и органических ионов) обусловлено загрязнениями и примесями. Эти же вещества вызывают появление влаги в коррозионных микроячейках даже в том случае, если поверхность защищена лакокрасочным покрытием. В этом случае накопление влаги под пленкой происходит в результате осмоса, в котором пленка выполняет роль мембраны. Скорость осмотического всасывания воды в микроячейки при прочих равных условиях зависит от природы и особенно количества электролитов, уже имеющихся в пленке и в микроячейках. [7]
Присутствие электролита может быть обусловлено наличием пигменте водорастворимых примесей. [8]
Присутствие электролитов в суспензии меняет схему адсорбции частиц на поверхности зерен твердых материалов. [9]
Присутствие электролитов приводит к возникновению высоких осмотических давлений, а при наличии мембран вызывает установление мембранного ( доннановского) равновесия ( см. гл. [10]
Присутствие электролитов, особенно многозарядных катионов, нежелательно, так как они вызывают коагуляцию осадка. Очень сильно они мешают при определениях с эозином, больше чем при определениях с флуоресцеином и дихлорфлуорес-цеином. [11]
В присутствии электролитов, способных пассивировать поверхность металла, наблюдается обратное явление - активная поверхность анода незначительна. Плотность тока на таких участках очень велика, что приводит к сильной анодной поляризации. Кривая анодной поляризации в последнем случае имеет сложный вид и подобна приведенной выше. [12]
В присутствии электролита, содержащего одноименный ион с одним из ионов труднорастворимого электролита, растворимость последнего уменьшается. ПР, представляющая собой произведение концентраций ( активностей) ионов, является при данной температуре постоянной величиной. Для увеличения полноты осаждения выделяемых из воды ионов необходимо вести процесс при некотором избытке осадителя. [13]
В присутствии электролита такая структура растравливается очень равномерно и медленно. Правильно отожженный материал не чувствителен к низкотемпературным нагревам и сохраняет свою высокую коррозионную стойкость в процессе эксплуатации изделий. [15]
Страницы: 1 2 3 4 5
