Присутствие - галоген
Cтраница 1
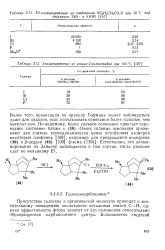 |
Элиминирование из гексил-2 - галогенидов при 100 С. [1] |
Присутствие галогена в органической молекуле приводит к значительному повышению кислотности остальных связей С - Н, однако эффективность фтора зависит от его положения относительно образующегося карбанионного центра. [2]
Присутствие галогенов, серы, фосфора в анализируемых веществах не оказывает влияния на результаты определений. [3]
Присутствие галогенов в фенильной группе, находящейся в положении 9, способствует образованию лактонной формы, причем эта тенденция возрастает во все большей степени по мере увеличения молекулярного веса галогенов. [4]
Присутствие галогенов в борановом ядре затрудняет диссоциацию из-за оттягивания электронов атомами галогена. В соответствии с этим, например, B10Cl8 ( N2) 2 реагирует с окисью углерода только выше 200 С. С другой стороны, наличие галогенов облегчает реакции, идущие через нуклеофильную атаку. Так, азид иона легко замещает группы N2fl Bi2Cl8 ( N2) 2, тогда как B10H8 ( N2) 2 реакция не идет. [5]
Возможность присутствия галогенов, тиоэфирных, эфирных и третичноаминных групп исключается сравнительно низким значением молекулярной массы при наличии бензольного кольца и алкильных радикалов. [6]
В присутствии галогенов ( С12, Вг2) или кислорода, которые играют роль промоторов, скорость нитрования увеличивается. При гетерогенном катализе ( на твердых катализаторах) существенно увеличивается скорость окисления. [7]
 |
Прибор для измерения небольших давлений пара при температуре ниже комнатной.| Колбочка для определения четкости точки плавления.| Давление в тройной точке. [8] |
В присутствии галогенов или других газов, реагирующих со ртутью, измерение давления проводят, используя упругие манометры. Другие возможные методы описаны в разд. [9]
В присутствии галогенов выпадают творожистые осадки серебряных солей: белый - хлорида, бледно-желтый - бромида, желтый - иодида. В отличие от бромида и иодида серебра хлорид серебра растворим в 12 % - ном растворе ( NH4) 2CO3 и в растворе аммиака и вновь выпадает в осадок при подкислении раствора. AgBr растворим в растворе аммиака частично, Agl - практически нерастворим. [10]
Анализу мешает присутствие галогенов и некоторых органических кислот. [11]
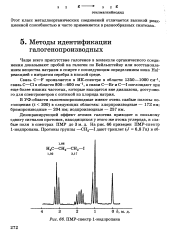 |
ПМР-спектр 1-иодпропана. [12] |
Чаще всего присутствие галогенов в молекуле органического соединения доказывают пробой на галоген по Бейлыптейну или восстановлением вещества натрием в спирте с последующим определением иона На1 - реакцией с нитратом серебра в кислой среде. [13]
Чаще всего присутствие галогенов в молекуле органического соединения доказывают пробой на галоген по Бейльштейну или восстановлением вещества натрием в спирте с последующим определением иона НаГ реакцией с нитратом серебра в кислой среде. [14]
 |
ПМР-спектр 1-иодпропана. [15] |
Страницы: 1 2 3 4