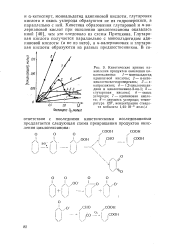
Притцков
Cтраница 1
Притцков 18 19 выделил концентраты гидроперекисей из окси-датев циклогексанона, 1-метилциклогексанона - 2, бутанона-2 и ди-н-пропилкетона. Строение кетогидроперекисей было подтверждено восстановлением в соответствующие кетоспирты. [1]
Притцков и Гробе 5 проводили исследование по окислению моноалкилциклогексанов и разложению образовавшихся гидроперекисей при температуре 100 С. В работе определены составы продуктов, полученных при радикальном и кислотном разложении гидроперекисей. Наибольший интерес представляют исследования Хоукинса 6 с сотрудниками по окислению ме-тилциклопентана и метилциклогексана, показывающие, что окислению подвергаются как третичный, так и вторичные углеродные атомы. [2]
Притцков отметил, что эти перекиси при действии тетраце-тата свинца выделяют кислород. [3]
Притцков 1819 выделил концентраты гидроперекисей из окси-датов циклогексанона, 1-метилциклогексанона - 2, бутанона-2 и ди-н-пропилкетона. Строение кетогидроперекисей было подтверждено восстановлением в соответствующие кетоспирты. [4]
Притцков отметил, что эти перекиси при действии тетраце-тата свинца выделяют кислород. [5]
Лангенбек и Притцков [81] установили факт, не согласующийся со схемой Рихе. Они нашли, что первичные спирты в условиях, при которых проводят окисление парафинов, окисляются преимущественно не в гомологичные жирные кислоты, а по метиленовым и метальным группам углеродного скелета, что приводит к образованию карбоновых кислот и оксикислот. [6]
Основываясь на своих исследованиях, Лангенбек и Притцков принимают, что первой стадией процесса является образование гидроперекисей; это согласуется с представлениями Рихе и других исследователей. [7]
 |
Содержание спиртов при неглубоком окислении н-додекана. [8] |
Этим и следует объяснить, почему Лангенбек и Притцков [6] в предложенной ими схеме реакции окисления парафиновых углеводородов не приводят первичных спиртов. [9]
Хок и Сасемил88 в продуктах термического разложения тет-ралилгидроперекиси при 130 С обнаружили а-тетралон и воду, а Притцков и Мюллер установили, что в присутствии солей металлов эта гидроперекись дает также а-тетралолш. Пока зано, что скорость разложения зависит от природы применяемого растворителя 12, что было подтверждено Робертсоном и Уотерсом95, которые изучили кинетику разложения в различных растворителях, включая тетралин и хлорбензол. Образование свободных радикалов при разложении было показано инициированием полимеризации добавленных мономеров. Продукты реакции, помимо а-тетралона ( 48 мол. [10]
Кинетика образования глутаровой и - валериановой кислот при окислении циклогексанона оказалась иной [40], чем это следовало из схемы Притцкова. Глутаровая кислота получается параллельно с моноальдегидом адипиновой кислоты ( а не из него), а н-валериановая и глутаровая кислоты образуются из разных предшественников. [12]
Что касается места первичной атаки углеводородов нормального строения, то, как показал в 1955 г. В. Притцков [216], здесь отсутствует преимущественное окисление какой-либо СН2 - группы. Вступление О2 в молекулу подчиняется законам статистического распределения. [13]
Поскольку при окислении постоянно образуются новые количества перекисей, этот процесс протекает автокаталитически. Вторая фаза реакции - распад гидроперекиси - тоже катализируется солями марганца, как это установили Лангенбек и Притцков. Итак, соли марганца являются катализаторами образования и распада гидроперекисей и можно принять, что последняя реакция тоже протекает по радикально-цепному механизму, поскольку фенолы и амины ее подавляют. Органические кислоты никак не влияют на скорость разложения перекисей. Интересно еще то, что происходящее при распаде гидроперекисей, например гидроперекиси тетралина, побочное образование спиртов в присутствии солей марганца как катализаторов больше, чем в случае некатализируемой реакции. [14]
Отличительной особенностью а-гидроперекиси циклогексанона, а также гидроперекисей многих других кетонов является их чувствительность к кислотам. При 90 и концентрации карбановых кислот 0 625 экв / л константа скорости распада а-гидропереккси циклогексанона составляет около 0 5 - 10 - 2 мин-1 и сопоставима с константой скорости распада в присутствии 0 01 % лаурината марганца. Как показал Притцков, константа скорости распада в присух ствии карбоновых кислот возрастает прямо пропорционально квадратному корню из их концентрации. [15]
Страницы: 1 2