Притяжение - электрон
Cтраница 3
Последний член появляется в результате одновременного притяжения электронов в молекуле к двум ядрам. Соотношение (5.8) показывает, что связь образуется лишь в том случае, если последний член достаточно велик, что бы скомпенсировать другие кулоновские члены противоположного знака. [31]
В последнем случае необходимо, чтобы притяжение электронов за счет их фононного обмена превышало их кулоновское отталкивание. Интересно проследить влияние дпэлектризашш на сверхпроводящий ФП. Диэлектризация определяет возможность образования куперовских пар при исследующем ( более низкотемпературном) сверхпроводящем переходе. Поскольку плотность электронных состояний на оставшейся части поверхности Ферми вблизи диэлектрической щели возрастает, вероятно, что именно диэлек-тризация может повысить температуру сверхпроводящего ФП. [32]
 |
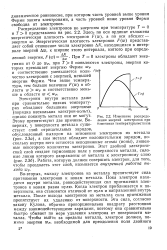
Сила F ( х, действующая на электрон, в зависимости от расстояния х [ Л. 6 - 24 ]. [33] |
На определенном расстоянии от поверхности сила Притяжения электрона становится меньше величины, получаемой по уравнению ( 6 - 3); она переходит через максимум и постепенно снижается до нуля по мере приближения рассматриваемой точки к внутренней области металла. [34]
Место разрыва может быть определено по относительному притяжению электрона радикалами, о чем будет говориться ниже. [35]
Чем больше радиус атома, тем меньше притяжение электрона к ядру при одинаковой величине его заряда; тем легче оторвать электрон от атома. Электроны можно не только отрывать, но и присоединять. Казалось бы, что электроны легче присоединить к тем атомам, которые прочнее удерживают свои электроны. [36]
При переходе к более тяжелым элементам сила притяжения электронов к ядру возрастает и размеры ближайших к ядру электронных облачков уменьшаются, но зато снаружи добавляются новые электроны, так что в целом размеры атома изменяются слабо. [37]
Почему в планетарной модели атома гравитационная сила притяжения электронов к ядру никакой роли не играет. [38]
Надо помнить, что, говоря о притяжении электрона к тому или иному атому, мы должны иметь в виду атом в том состоянии, в котором он находится в данной молекуле. Пользование шкалой Полинга не всегда дает логически безупречные результаты. [39]
Вообще говоря, поскольку речь идет о притяжении электрона ядром, значения а ( а также Р) должны быть отрицательны. Но если в качестве нуля принять а в бензоле, то интеграл а может быть численно и положительным, если электроотрицательность соответствующего атома меньше электроотрицательности атома углерода в бензоле. [40]
 |
Изменение распределения энергий электронов при изменении температуры металла. [41] |
Во-вторых, выходу электронов из металла препятствует сила притяжения электронов к ионам металла. Пока электрон находится внутри металла, равнодействующая сил притяжения электронов к ионам равна нулю. Когда электрон приближается к поверхности, она становится отличной от нуля и направленной внутрь металла. После выхода электронов из металла сила притяжения препятствует их удалению от поверхности. Эта сила, согласно закону Кулона, обратно пропорциональна квадрату расстояния между взаимодействующими зарядами, поэтому она сравнительно быстро убывает по мере удаления электрона от поверхности металла. [42]
В (16.7) первые четыре члена обозначают потенциальную энергию притяжения электронов 1 и 2 к ядрам А и В соответственно, пятый член - потенциальную энергию взаимного отталкивания электронов 1 и 2, последний член - энергию отталкивания ядер. Аналогично строится гамильтониан и для многоатомных молекул. Для молекулы, так же как и для атома, точное решение уравнения (16.1) возможно лишь для системы, содержащей один электрон - для молекулярного иона типа НЬ. [43]
В (16.7) первые четыре члена обозначают потенциальную энергию притяжения электронов 1 и 2 к ядрам А и В соответственно, пятый член-потенциальную энергию взаимного отталкивания электронов 1 и 2, последний член - энергию отталкивания ядер. Аналогично строится гамильтониан и для многоатомных молекул. [44]
Пониженная прочность связей b и Ь1 является следствием притяжения электронов по направлению к связанным двойной связью атомам углерода. Это притяжение в определенных условиях может быть настолько сильным, что ослабленная связь разрушается. С увеличением отдаленности от двойной связи постепенно уменьшается различие в прочности вязей. [45]
Страницы: 1 2 3 4