Молекулярное притяжение
Cтраница 2
Под действием сил молекулярного притяжения поверхностно-активные вещества выпадают из водного раствора и оседают на твердой поверхности пористой среды. Этот процесс в значительной мере определяется удельной поверхностью и адсорбционной активностью поверхности пористой среды. [16]
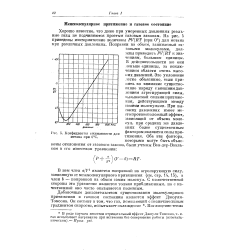 |
Коэфициенты сжимаемости для метана при 0 С. [17] |
Добавочным доказательством существования молекулярного притяжения в газовом состоянии является эффект Джоуля-Томсона. [18]
В случае взвешивания молекулярного притяжения опасны как быстрые, так и медленные изменения в датчике, так как требуется достаточно длительное устойчивое положение равновесия коромысла, чтобы замерить одновременно зазор между поверхностями и соответствующую ему силу тока. Это особенно существенно при измерениях на воздухе, ибо в этом случае ползание коромысла вызывает силы сопротивления, зависящие от вязкости воздуха и искажающие измеряемые силы. [19]
На неодинаковой величине молекулярного притяжения друг к другу различных веществ ( что, между прочим, проявляется в неодинаковом смачивании различных твердых тел различными жидкостями), а также на влиянии примеси различных солей на поверхностное натяжение растворителя основаны флотационные1) процессы, играющие важную роль в технике обогащения различных руд и в разделении различных металлов друг от друга. [20]
Так как силы молекулярного притяжения в поверхностном слое жидкости ( и твердого вещества также) не скомпенсированы, в нем появляется свободная поверхностная энергия. Количественно эту энергию характеризуют удельной величиной, т.е. величиной, отнесенной к единице поверхности. Эта энергия, обозначаемая греческой буквой о, является основной характеристикой поверхностного слоя жидкости или твердого вещества. [21]
В газах силы молекулярного притяжения гораздо меньше, чем в жидкости, и силы поверхностного натяжения не играют никакой роли. Отсутствие поверхностного натяжения является одним из характерных признаков, отличающих газообразное со. [22]
Само существование сил молекулярного притяжения не подлежит никакому сомнению. Чрезвычайно простыми опытами нетрудно показать способность твердых тел слипаться под влиянием этих сил. [23]
На действии сил молекулярного притяжения основано образование маленьких комочков или агрегатов из мельчайших частиц тонких порошков. [24]
Итак, силы молекулярного притяжения могут действовать между двумя шариками, находящимися или даже не находящимися в контакте. Если мы вспомним, что сила тяжести, действующая на шарик и пропорциональная его объему, должна меняться пропорционально кубу радиуса, то мы легко придем к выводу, что, по мере того как мы берем все более мелкие частицы, равнодействующая силы молекулярного взаимодействия их будет убывать медленнее, чем вес каждого из них. В результате для частиц, радиус которых достаточно мал ( приблизительно меньше микрона), силы притяжения берут перевес над силами тяжести. Поэтому такого рода частицы могут слипаться и, образуя комки, не разрушаться под действием силы тяжести отдельных частиц. Любопытно отметить, что в ряде случаев ( например, для некоторых сортов сажи) эти комки имеют весьма правильную, шарообразную форму. [25]
Под действием сил молекулярного притяжения ПАВ выпадают: водного раствора и оседают на твердой поверхности пористой среды. [26]
Явление притираемости объясняется молекулярным притяжением в присутствии тончайших слоев смазочной пленки. Такая толщина пленки является наиболее благоприятной для притираемости плиток при обычном качестве отделки их измерительных поверхностей. [27]
 |
Плоскопараллельные концевые меры. [28] |
Притираемость плиток объясняется молекулярным притяжением доведенных плоских поверхностей, покрытых тончайшей жидкостной пленкой. [29]
Такое объединение частиц силами молекулярного притяжения может привести к образованию сплошной структурированной системы, обладающей фазовой устойчивостью ( см. гл. [30]
Страницы: 1 2 3 4