Межионное притяжение
Cтраница 1
Межионное притяжение стремится втянуть ионы внутрь раствора, частично освобождая от них поверхность раствора и тем самым уменьшая задерживающее влияние растворенных частиц ( ионов) на скорость испарения растворителя. Благодаря этому понижение давления пара ( и изменения других свойств растворов, связанных с давлением пара) будет меньше по сравнению с тем, если бы ионы действовали независимо друг от друга. [1]
Указанное межионное притяжение вызывает отклонения в поведении реальных растворов аналогично тому, как межмолекулярное притяжение в реальных газах влечет за собой отступления их поведения от законов идеальных газов. [2]
Более сильное межионное притяжение между адсорбированными ионами решетки и противоионами устанавливается по следующим признакам: а) по более низкой растворимости; б) по меньшей степени диссоциации; в) большей степени ковалентно-сти и г) большей электрической поляризуемости аниона и поляризующей силы катиона. [3]
Более сильное межионное притяжение между адсорбированными ионами решетки и противоионами устанавливается по следующим признакам: а) по более низкой растворимости; б) по меньшей степени диссоциации; в) большей степени ковалентности и г) большей электрической поляризуемости аниона и поляризующей силы катиона. [4]
С увеличением концентрации увеличииается межионное притяжение и начинает сказываться изменение степени сольватации ионов и степени ионизации электролита. В результате перемещение ионов затрудняется, что приводит к уменьшению эквивалентной электропроводности. [5]
Причина этого находится в межионном притяжении электролитов. Явление ускорения реакций, связанное со смещением равновесия посредством изменения среды, окружающей ионы, названо вторичным солевым эффектом. [6]
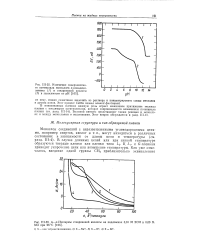 |
Изменение поверхностного потенциала монослоев я-нонадеци-ламина ( 1 и стеариновой кислоты ( 2 в зависимости от рН. [7] |
В ионизованных пленках важную роль играет межионное притяжение молекул пленки с вводимыми электролитами, которое сопровождается изменением потенциала пленки ( см. разд. Большой интерес представляют также реакции в монослоях и между монослоями и подложками. Этот вопрос обсуждается в разд. [8]
 |
Удельное сопротивление и удельная электропроводность некоторых материалов. [9] |
При более высоких концентрациях электропроводность вновь уменьшается, поскольку межионное притяжение затрудняет движение ионов в растворе. [10]
В очень разбавленных растворах расстояние между ионами настолько увеличивается, что межионное притяжение приближается к нулю, подвижность ионов возрастает и вещество диссоциирует практически полностью. [11]
В очень разбавленных растворах расстояние между ионами настолько увеличивается, что межионное притяжение приближается к нулю, подвижность ионов возрастает и вещество диссоциирует практически полностью. [12]
Дополнительные аргументы в пользу соотношения Нернста - Эйнштейна дает теория Дебая - Хюккеля, рассматривающая межионное притяжение ( разд. [13]
Дополнительные аргументы в пользу соотношения Нернста - Эйнштейна дает теория Дебая - Хюккеля, рассматривающая межионное притяжение ( разд. [14]
В очень разбавленных растворах ( особенно слабых электролитов) расстояние между ионами настолько увеличивается, что межионное притяжение приближается к нулю, подвижность ионов возрастает и вещество диссоциирует практически полностью. [15]
Страницы: 1 2