Межионное притяжение
Cтраница 2
Увеличение растворимости электролита вследствие увеличения ионной силы раствора вызывается, согласно теории сильных электролитов, изменением подвижности ионов, которое обусловлено межионным притяжением ( см. § 6) и связано с изменением величины коэффициента активностей. [16]
Согласно теории сильных электролитов, то обстоятельство, что сильные электролиты не вполне подчиняются закону действия масс в его классической форме, объясняется изменением подвижности ионов; изменение подвижности ионов, как уже говорилось, обусловлено межионным притяжением ( см. стр. [17]
Второе допущение в упрощенном законе Дебая - Хюккеля заключается в том, что наряду с действующими электростатическими силами, в растворе существует также случайное, тепловое движение ионов, которое нарушает ориентацию противоположно заряженных частиц, вызванную межионным притяжением. Дебай и Хюккель упростили свою гипотетическую модель растворов электролитов и в некоторых других аспектах, предполагая, что ионы не могут быть поляризованы и поэтому имеют сферическое распределение заряда, а сами ионы предложили рассматривать как точечные заряды. Кроме того, упрощенный закон Дебая - Хюккеля предполагает, что диэлектрическая проницаемость раствора электролита является постоянной и не зависит от реальной концентрации растворенного вещества, поэтому во всех расчетах можно использовать диэлектрическую проницаемость чистой воды. [18]
Межионное притяжение вызывает отклонения в поведении реальных растворов аналогично тому, как межмолекулярное притяжение в реальных газах влечет за собой отступления их поведения от законов идеальных газов. [19]
Объяснение того факта, что сильные электролиты, подобные бромистому калию, вызывают меньшее понижение температуры замерзания, нежели понижение, вычисленное при допущении полной диссоциации, заключается в том, что существуют мощные электрические силы, действующие между ионами, и эти силы снижают активность ионов, в результате чего свойства ионных растворов отличаются от свойств идеальных растворов во всех случаях, за исключением крайне разбавленных растворов. Межионное притяжение снижает активность ионов до значения, меньшего, чем их концентрация. [20]
Межионное притяжение вызывает отклонения в поведении реальных растворов аналогично тому, как межмолекулярное притяжение в реальных газах влечет за собой отступления их поведения от законов идеальных газов. [21]
Но в случае меньших анионов межионное притяжение возрастает, и такие соли, хотя и диссоциируют при очень малых концентрациях, при более высоких образуют ионные пары. [22]
Указанное явление известно под названием солевого эффекта. Увеличение растворимости электролита за счет увеличения ионной силы раствора, неподчинение сильных электролитов закону действия масс в его классической форме объясняется, согласно теории сильных электролитов, изменением подвижности ионов, которое обусловлено межионным притяжением ( см. § 10, стр. [23]
Согласно этой теории, противоположно заряженные ионы в растворе притягиваются друг к другу. Отрицательные ионы окружают себя атмосферой положительных ионов, и наоборот. Межионное притяжение стремится втянуть ионы внутрь раствора, частично освобождая от них поверхность раствора и тем самым уменьшая задерживающее влияние растворенных частиц ( ионов) на скорость испарения растворителя. Благодаря этому понижение давления пара будет меньше по сравнению с тем, которое можно было ожидать, если бы ионы действовали независимо друг от друга. Понижение давления пара находится в тесной связи с другими свойствами раствора, такими, как осмотическое давление, понижение точки замерзания и повышение точки кипения. В более концентрированных растворах поэтому благодаря возрастанию межионного притяжения наблюдается уменьшение осмотического давления, а также уменьшение депрессий точек замерзания и кипения раствора против ожидаемых величин. [24]
Под влиянием приложенной разности потенциалов равномерность распределения ионов нарушается, силы, действующие между ними, перестают уравновешивать друг друга и благодаря возникновению тормозящих сил уменьшается подвижность ионов. В более концентрированных растворах, кроме того, важным фактором изменения подвижности ионов становится истинный диаметр ионов благодаря частым столкновениям катионов и анионов, движущихся в противоположных направлениях. При большом разведении межионное притяжение незначительно, и ионы движутся с максимальными скоростями, не зависящими от дальнейшего разведения. [25]
Как было указано выше, для сильных электролитов понятие степени диссоциации лишено смысла и особенно в тех случаях, когда само вещество электролита в твердом состоянии состоит из ионов. В растворах сильных электролитов вследствие высокой концентрации ионов значительную роль играет электростатическое взаимодействие между ними. При увеличении концентрации сильного электролита интенсивное межионное притяжение приводит к большему связыванию ионов и к изменению свойств растворов в направлении, аналогичном уменьшению степени диссоциации слабых электролитов, поэтому для сильных электролитов вводится величина кажущейся степени диссоциации. Наблюдающиеся отклонения от закона действия масс, которыми вызвано непостоянство константы диссоциации при разведении, могут быть компенсированы подбором величин эффективной концентрации. При подстановке вместо обычных концентраций величин эффективных концентраций, которые называются а к-тивностями ( Льюис, 1908 г.), возможно применение закона действия масс к растворам сильных электролитов и к более концентрированным растворам слабых электролитов. [26]
Активностью иона или молекулы называется его действующая концентрация. Эта концентрация, если ее ввести в уравнение закона химического равновесия, точно выражает влияние иона или молекулы на установление равновесия. Величина активности близка к величине молярной концентрации при увеличивающемся разбавлении раствора, так как при этих условиях ионы все больше удаляются друг от друга и, следовательно, межионное притяжение уменьшается. [27]
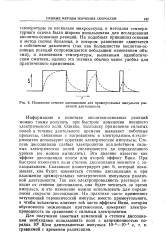 |
Изменение степени диссоциации для прямоугольных импульсов различной длительности. [28] |
Однако, поскольку применение сильных полей в течение длительного времени вызывает побочные процессы, связанные с нагреванием и электролизом, в экспериментах используют короткие электрические импульсы. Это явление известно как эффект диссоциации полем или второй эффект Вина. При быстром изменении поля степень диссоциации меняется с запаздыванием. Сказанное иллюстрирует рис. 6, который показывает, как будет изменяться степень диссоциации а при наложении прямоугольных электрических импульсов различной длительности. Так как электропроводность раствора зависит от степени диссоциации, она будет меняться за время импульса, и это изменение можно использовать для определения скорости диссоциации. На практике часто применяют затухающий гармонический импульс вместо прямоугольного, а чтобы исключить влияние той части эффекта Вина, которая обусловлена межионным притяжением, измеряют электропроводность по сравнению с сильным электролитом. [29]
Страницы: 1 2