Взаимное притяжение
Cтраница 2
Взаимное притяжение разноименно заряженных и отталкивание одноименно заряженных тел не оказывают заметного влияния на производственные операции, если зарядившиеся тела имеют значительные размеры и массу. Однако при переработке тонких пленок, нитей, частиц сыпучих и мелкодисперсных материалов силы электростатического взаимодействия могут вызывать нежелательные явления. Так, при чешуировании жирных кислот взаимное отталкивание заряженных частиц столь значительно, что некоторые из них оседают по пути и не попадают в бункер. Кроме того, частицы, попавшие в бункер, налипают на его стенки, что затрудняет разгрузку бункера. [16]
Взаимное притяжение нуклонов в ядре приводит к тому, что, находясь в поверхностном слое ядра, нуклоны, подобно молекулам поверхностного слоя жидкости, оказываются в несколько особых условиях, что вызывает существование своего рода поверхностного натяжения ядра. Вследствие этого деформации ядра, связанные с увеличением его поверхности, требуют затраты энергии; наиболее устойчивым является такое состояние, когда ядро обладает наименьшей поверхностью. [17]
Взаимное притяжение указанных ионов обеспечивает достаточное их приближение друг к другу и может сопровождаться явлениями миграции ионов брома из одной внутренней сферы в другую. [18]
Взаимное притяжение частиц пигмента во фталоцианиновом синем происходит в основном за счет дисперсионных сил, в то время как в случае периленового красного приходится дополнительно считаться с действием полярных сил ( диполь, водородные мостики), определяющих соответственно большую работу диспергирования. Поэтому фталоцианины в ярковыраженных полярных средах, например в воде, будут диспергироваться довольно плохо, так как взаимодействие между молекулами среды сильнее ( водородные мостики), чем взаимодействие молекул среды с неполярной поверхностью пигмента. [19]
Взаимное притяжение частиц пигмента во фталоцианиновом синем происходит в основном за счет дисперсионных сил, в то время как в случае периленового красного приходится дополнительно считаться с действием полярных сил ( диполь, водородные мостики), определяющих соответственно большую работу диспергирования. Поэтому; фталоцианины в ярковыраженных полярных средах, например в воде, будут диспергироваться довольно плохо, так как взаимодействие между молекулами среды сильнее ( водородные мостики), чем взаимодействие молекул среды с неполярной поверхностью пигмента. [20]
Взаимное притяжение противоположно заряженных ионов, в результате которого возникает молекула, носит электростатический характер. [21]
Такое взаимное притяжение описано в 9 и 8.10. Наблюдаемая тенденция соседних магнитных узлов ( силовых трубок) сближаться друг с другом и сливаться в поры и солнечные пятна может быть прямым следствием гидродинамических воздействий на всплывающие трубки. [22]
 |
Взаимное положение ного отталкивания молекул уже полярных молекул в жидкости. ПРИ сближении их в таком поло. [23] |
Если взаимное притяжение между молекулами относительно невелико, то образовавшиеся комплексы вновь распадаются под действием теплового движения других молекул. Если же взаимное притяжение значительно, то распада комплексов может не происходить, и в этом случае жидкость будет содержать подобные комплексы, состоящие из различного числа молекул. Повышение температуры, усиливая тепловое движение, должно способствовать большему распаду комплексов. [24]
Если взаимное притяжение адсорбированных молекул с заполнением1 адсорбционной фазы значительно возрастает, - щ оДно - компонентное заполнение адсорбционного пространства - лоргащь. [25]
Силы взаимного притяжения препятствуют разлетанйю молекул газа и, следовательно, действуют в том же направлении, что и внешнее давление р, удерживающее газ в данном объеме. [26]
Силы взаимного притяжения ( а также отталкивания) молекул, в том числе силы, действующие между цепями молекул полимеров, называются межмолекулярными силами, или вторичными силами, или силами Ван-дер - Ваальса. [27]
 |
Схема для вывода основного уравнения кинетической теории. [28] |
Силы взаимного притяжения между молекулами настолько малы, что ими можно пренебречь. [29]
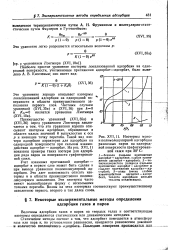 |
Изотермы моно-и полимолекулярной адсорбции различных паров на однородной поверхности графитирован-ной сажи при 20 С. [30] |
Страницы: 1 2 3 4