Взаимное притяжение
Cтраница 3
Учет взаимных притяжений адсорбат - адсорбат в первом слое может быть сделан и при выводе уравнения полимолекулярной адсорбции. Это дает возможность описать изотермы и в области преимущественно полимолекулярного заполнения. [31]
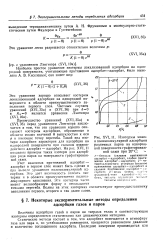 |
Изотермы моно-и полимолекулярной адсорбции различных паров на однородной поверхности графитирован-ной сажи при 20 С. . [32] |
Учет взаимных притяжений адсорбат - адсорбат в первом слое может быть сделан и при выволе уравнения полимолекулярной адсорбции. Это дает возможность описать изотермы и в области преимущественно полимолекулярного заполнения. Эти изотермы часто имеют волнообразную форму с несколькими точками перегиба. Волны на этих изотермах соответствуют преимущественному заполнению первого, второго и так далее слоев. [33]
Вследствие взаимного притяжения в рассматриваемом случае все заряды располагаются только на внутренних поверхностях пластин. Величина а, характеризующая распределение заряда по поверхности, называется поверхностной плотностью заряда. [34]
Силы взаимного притяжения между молекулами настолько малы, что ими можно прснсиречь. [35]
Силы взаимного притяжения препятствуют разлетанию молекул газа и, следовательно, действуют в том же направлении, что и внешнее давление р, удерживающее газ в данном объеме. Чтобы учесть действие этих сил, достаточно в первом приближении прибавить к внешнему давлению р некоторый добавочный член, который называется внутренним или молекулярным давлением и обозначается рмл. [36]
Силы взаимного притяжения сушествуют и в реальном газе, только они намного меньше, чем в жидкости, вследствие меньшей плотности газа. Его называют внутренним давлением. [37]
Силы взаимного притяжения между молекулами газа становятся заметными при высоких давлениях и низких температурах, когда расстояния между молекулами уменьшаются. [38]
 |
К объяснению принципа действия синхронного двигателя. [39] |
Силы взаимного притяжения в этом случае направлены по радиусам. [40]
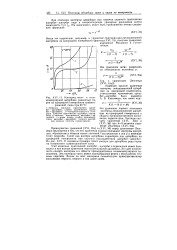 |
Изотермы моно - и поли-молекулярной адсорбции различных паров на однородной поверхности графити-рованной сажи при 20 С. [41] |
Учет взаимных притяжений адсорбат-адсорбат в первом слое может быть сделан и при выводе уравнения полимолекулярной адсорбции. Это дает возможность описать изотермы и в области преимущественно полимолекулярного заполнения. Эти изотермы часто имеют волнообразную форму с несколькими точками перегиба. Волны на этих изотермах соответствуют примущественному заполнению первого, второго и так далее слоев. [42]
 |
Схема диссоциации полярной молекулы на ионы. [43] |
Силы взаимного притяжения возникают между ионами молекулы и диполями воды. В результате этого притяжение между противоположными ионами в молекуле электролита ослабевает и молекула распадается на ионы. [44]
Силы взаимного притяжения препятствуют разлетанию молекул газа и, следовательно, действуют в том же направлении, что и внешнее давление р, удерживающее газ в данном объеме. [45]
Страницы: 1 2 3 4