Причина - диссоциация
Cтраница 1
Причины диссоциации анксиолитической и других видов активности у транквилизаторов / 3-карболинового ряда различны. Более вероятно, по-видимому, сочетание у 0-карболинов свойств транквилизаторов и антидепрессантов [ 4 Три - и тетрациклические антидепрессанты уменьшают седативныи ги-полокомоторный) и снотворный эффекты бензодиазепиновых трап - в. [1]
Причина диссоциации заключается в том, что молекула воды имеет большой дипольный момент ( ре6 ЫО-30 Кл - м), вследствие чего на расстояниях, имеющих порядок расстояния между молекулами в жидкостях ( гяз5 10 - м), вокруг нее возникает сильное электрическое поле. [2]
Причина диссоциации заключается в том, что молекула воды имеет большой дипольный момент ( ре6 Ь IQ-M Кл - м), вследствие чего на расстояниях, имеющих порядок расстояния между молекулами в жидкостях ( г ж А 10 - 10 м), векруг нее возникает сильное электрическое поле. [3]
Причиной диссоциации является притяжение, испытываемое молекулами уксусной кислоты со стороны близлежащих молекул воды. Вследствие этого центры тяжести отрицательных и положительных электрических зарядов в молекуле Н2О не совпадают, а находятся в двух различных точках простру ранства. Такие молекулы называют ди-польными, или диполями. Подобные диполи, несмотря на их электронейтральность в целом, могут оказывать электростатическое молекуланС0роения воздействие на окружающие их ионы или 2 диполи. [4]
Но электрический ток никогда не является причиной диссоциации. [5]
Самым серьезным недостатком теории Аррениуса является то, что она не объясняет причину диссоциации электролитов на ионы. [6]
Теория электролитической диссоциации Аррепиуса, объяснившая многие явления, связанные с электропроводностью растворов, оставляла открытым вопрос о причинах диссоциации электролита и условиях существования ионов в растворе. [7]
Рассмотрим диссоциацию слабых электролитов на примере уксусной кислоты. Причиной диссоциации является притяжение, испытываемое молекулами уксусной кислоты со стороны близлежащих молекул воды. Вследствие этого электрические центры тяжести отрицательных и положительных зарядов в молекуле Н2О не совпадают, а находятся в двух различных точках пространства. [8]
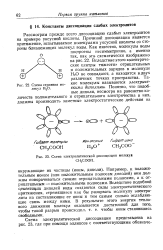 |
Схема строения молекул Н2О.| Схема электролитической диссоциации молекул СН3СООН. [9] |
Рассмотрим прежде всего диссоциацию слабых электролитов на примере уксусной кислоты. Причиной диссоциации является притяжение, испытываемое молекулами уксусной кислоты со стороны близлежащих молекул воды. [10]
Вследствие резонанса с хиноидными структурами, в которых холостые электроны находятся у орто - и параатомов углерода, эти радикалы можно, конечно, описать так же хорошо, как содержащие трехвалентный углерод. Причиной большей диссоциации соединений этого последнего типа даже в отсутствие особенно больших стерических взаимодействий является, вероятно, то, что работа, требуемая для разрыва связи азот-азот, меньше, чем для разрыва связи углерод-углерод, и поэтому одинаковая стабилизация радикала, вызванная резонансом, приводит к большему результирующему эффекту. Аналогично, гексаарилтет-разаны диссоциируют на триарилгидразилы. [11]
Большие центробежные поля в ультрацентрифуге являются одной из причин диссоциации рибосомных белков при их выделении методом зонного центрифугирования. Это интересное явление, обнаруженное Бреслером [43], указывает на влияние гидростатического давления на диссоциацию олигомер-ных белков и рибосом на субъединицы. [12]
Формула Шленка ( выведенная им, кстати сказать, на основе аналогии между строением молекулы и планетной системы), однако, не была принята как серьезная основа для дальнейших исследований. В то же время его работа особенно остро поставила вопрос о причинах диссоциации гексаарилэтанов. Но, конечно, природа этого фактора могла быть понята и изучена гораздо позднее. [13]
Аррениус считал, что распад молекул электролитов на ионы происходит самопроизвольно, причины диссоциации не были вскрыты, растворитель представлялся безразличной средой, не оказывающей влияния на процесс диссоциации. [14]
Аррениус считал, что распад молекул электролитов на ионы происходит самопроизвольно, причины диссоциации не были вскрыты, растворитель представлялся безразличной средой, не оказывающей влияния на процесс диссоциации. В развитии теории электролитической диссоциации большую роль сыграл И. А. Каблуков, много лет занимавшийся изучением неводных растворов. [15]
Страницы: 1 2