Про-тивоионы
Cтраница 3
В определении свойств жестких и мягких кислот и оснований роль растворителя гораздо важнее, чем это кажется на первый взгляд. В результате эти ионы, взятые отдельно, имеют орбитальные характеристики, которые мы приписывали мягким системам. Плотная положительная сольватная оболочка понижает ВЗМО малых анионов. Отрицательные про-тивоионы повышают энергию НВМО малых катионов. Малые ионы, кроме того, частично приобретают жесткость в начале кислотно-основной реакции при прямом взаимодействии с субстратом, кулоновское поле которого оказывает стабилизирующее влияние, подобное влиянию протонных растворителей. С другой стороны, в комплексах катиона Li с краун-эфирами или криптандами он имеет характер мягкой кислоты, и реакция контролируется граничными орбиталями благодаря низкой НВМО иона, который реагирует так, как будто он изолированный [35] и больший по размерам, чем на самом деле. [31]
В зависимости от знака заряда функциональных групп ионообменные смолы являются катионитами или анионитами. Катиониты содержат кислотные функциональные группы [ - SO3 -, - СО2 - РО32 -, - N ( CH2CO2 -) 2J, поэтому каркас катионита, несущий фиксированные отрицательные заряды, заряжен отрицательно. Отрицательные заряды каркаса компенсируются положительными зарядами противоионов, так что в целом катионит остается электронейтральным. Однако про-тивоионы, в данном случае катионы, в отличие от функциональных групп каркаса обладают подвижностью-и могут переходить в раствор в обмен на эквивалентное количество ионов из раствора. Этот обмен приводит к установлению подвижного равновесия между ионами, находящимися в фазе смолы и ионами в растворе. [32]
На их поверхности адсорбированы молекулы белков, аминокислот и ионы электролитов. Все они сообщают эритроцитам опре. С-потенциал), а про-тивоионы создают некоторый диффузный слой. При различных патологических процессах в организме, когда в крови увеличивается содержание некоторых видов белков ( либо особого глюкопротеида, относящегося к а-глобулинам, либо при инфекционных заболеваниях, f - глобулинов) происходит процесс, очень напоминающий ионообменную адсорбцию: место ионов электролитов на поверхности эритроцитов занимают белки, заряд которых ниже, чем у суммы замещенных ими ионов. Оседание эритроцитов протекает сходно с процессом седиментации гидрофобного коллоида. [33]
В этих условиях связывание противоположно заряженных ионов невозможно. При наличии мицелл положение меняется. При числе агрегации п первичное ядро мицеллы взаимодействует с отдельным ионом с энергией в п раз большей чем по формуле (13.1), и если при п 1 эта энергия на порядок меньше kT, то при п 100 - на порядок больше. Такое мицеллярное ядро будет связывать про-тивоионы. [34]
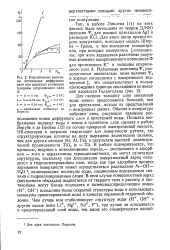 |
Рассчитанные величины потенциала диффузного слоя при заданных значениях толщины штерновского слоя А. [35] |
Обычно в литературе избегают схем, рисующих взаимное расположение ионов диффузного слоя и пристенной воды. В работе подчеркивается, что процессы, ведущие к возникновению заряда - диссоциация и адсорбция - хотя и неразличимы термодинамически, но могут отличаться структурно, поскольку при диссоциации поверхностный заряд находится в гидроксилированном слое, тогда как при адсорбции процесс заряжения поверхности может осуществляться радикалами М - ОН - Н2О 1, включающими молекулы воды, соединенные водородными связями с гидроксилированным слоем. В этом случае поверхностный заряд ( внутренняя обкладка) выдвигается от твердого тела в раствор и про-тивоионы могут ближе подходить к потенциалопределяющим ионам ( Н, ОН -) вследствие более открытой структуры воды и использовать молекулы ориентированной воды в качестве первичной гидратной оболочки. [36]
Как правило, набухание ионита протекает обратимо и характеризуется равенством между осмотическим давлением внутреннего раствора, с одной стороны, и натяжением эластичной сетки полимера, с другой. Осмотическое давление почти полностью обусловлено противоионами. Можно предположить поэтому, что обмен противо-ионов оказывает существенное влияние на процесс набухания. При этом решающее значение имеет число осмотически активных ионов на единицу веса ионита. Следовательно, однозарядные про-тивоионы должны вызывать более сильное набухание, чем многозарядные. Можно также утверждать, что добавление электролита к внешнему раствору должно приводить к уменьшению набухания, если степень диссоциации ионита считать постоянной. Проведенные Самуэльсоном [102, 104] эксперименты над сульфированными катионитами различных типов показали, что указанные закономерности, за редкими исключениями, хорошо выполняются. [37]
 |
Выходная кривая ti л. [38] |
Набухание зависит от свойств ионита и водного раствора, в который он погружен. Причиной набухания является, как указано выше, наличие в структуре смол гидрофильных ионо-генных групп. Чем их больше ( чем выше емкость смолы), тем более склонен ионит к набуханию. При малом числе поперечных связей в матрице ионита набухание может достичь больших величин. Таким образом, набухший ионит представляет собой систему, в которой ионогенные группы и про-тивоионы растворены в проникшей ионит воде. [39]
Страницы: 1 2 3