Четвертая пробирка
Cтраница 1
Четвертая пробирка - пустая, помещается в водяную баню с температурой 4 - для конденсации паров уксусной кислоты. [1]
Четвертая пробирка служит для сравнения полученных окрасок. [2]
В четвертую пробирку добавляют 5 - 8 капель 10 % - ного раствора едкого натра и нагревают до кипения: осадок не выпадает, поскольку мицеллы заряжены отрицательно. [3]
В четвертую пробирку вливают 0 55 мл 0 01 % - ного эталонного раствора сульфата атропина. Объем жидкости во всех пробирках доводят 1 % - ным раствором соляной кислоты до 5 мл и добавляют в каждую пробирку по 2 капли 3 % - ного раствора фосфорновольфрамовой кислоты. Образовавшееся помутнение измеряют с помощью нефелометра и содержание алкалоидов вычисляют по предварительно построенному калибровочному графику или же сравнивают со шкалой эталонных пробирок, в которых известно количество алкалоидов. [4]
В четвертую пробирку, так же как и в третью, добавляют 0 5 мл 10 % - ного раствора СН3СООН и несколько капель насыщенного раствора NaCl. При нагревании образуется осадок. Выпадение осадка в этом случае связано с тем, что добавляемый хлорид натрия, как и другие соли щелочных и щелочноземельных металлов, адсорбируется на белковых частицах, делая их электронейтральными ( снимая заряд) и понижая их устойчивость в растворе. Кроме того, при достаточно большой концентрации солей происходит дегидратация белковых мицелл. [5]
В четвертую пробирку наливают 0 5 мл раствора реагента и 0 06 мл дистиллированной воды. Затем пробирки встряхивают одновременно в течение 1 минуты и отмечают изменение окраски в органическом слое. NaOH, I M СН3СООН, ледяной СНзСООН, 5 % - ного НС1, HNO3 ( 1: 2) и H2SO4 ( 1: 3) и отмечают переход окраски в органическом слое. [6]
В четвертую пробирку вводят 2 - 3 капли дистиллированной воды и нагревают на водяной бане, осадок растворяется. [7]
В четвертую пробирку - контрольную - наливают 5 мл диметилформамида. Во все четыре пробирки приливают по 0 05 мл буферного раствора изобутиламина, 0 2 мл раствора бис-салицилальэтилендиамина, встряхивают и оставляют на 5 минут для образования комплекса магния с реагентом. [8]
В четвертую пробирку прибавить сухую соль хлористого аммония и энергично перемешать стеклянной палочкой. Окраска раствора по мере растворения NH4C1 заметно ослабляется. [9]
В четвертую пробирку к 1 мл н-гексана приливают 1 мл раствора перманганата калия ( КМпОД После встряхивания содержимого пробирки отмечают, что изменений не происходит, раствор не обесцвечивается, т.е. реакция не идет. [10]
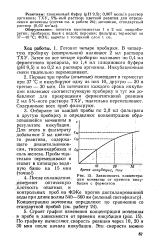 |
Зависимость концентрации мочевины of. времени Инкубации с ферментом. [11] |
В четвертую пробирку ( контрольная) наливают 2 мл раствора ТХУ. Затем во все четыре пробирки наливают по 0 4 мл ферментного препарата, по 1 4 мл глицинового буфера ( рН 9 5) и по 0 2 мл раствора аргинина. Инкубационные смеси тщательно перемешивают. [12]
Добавляют в четвертую пробирку около 0 5 мл 10 % уксусной кислоты, несколько капель насыщенного раствора хлористого натрия и нагревают. [13]
К раствору яичного белка в четвертой пробирке добавляют 1 - 2 капли 10 % - ного раствора уксусной кислоты, 1 каплю насыщенного раствора хлорида натрия и нагревают. Выпадает осадок белка, так как происходит нейтрализация заряда на частицах белка. [14]
 |
Шкала для определения изоэлектрической точки белка. [15] |
Страницы: 1 2 3 4