Проведение - изомеризация
Cтраница 4
Активные центры гидрирования-дегидрирования в отсутствие водорода быстро отравляются в результате распада на них углеводородов до элементов, поэтому процесс нужно проводить под давлением водорода. Кроме того, катализатор, имеющий только кислотную активность, при проведении изомеризации смесей - парафинов с олефинами быстро отравляется коксом как в присутствии водорода, так и без него. При нанесении на такой кислотный катализатор металла, катализирующего гидрирование-дегидрирование, и под давлением водорода закоксовывание кислотных центров резко замедляется, следовательно, гидрирующие ( дегидрирующие) активные центры не только обеспечивают промежуточное образование олефинов, но и предохраняют соседние кислотные активные центры от закоксовывания. [46]
Миграция ацильного остатка в ароматических соединениях изучена плохо. К настоящему времени еще не найдены общие условия и катализаторы, пригодные для проведения изомеризации различных типов аци-лированных ароматических соединений. В известной мере это объясняется склонностью ароматических кетонов к реакциям конденсации под влиянием кислотных катализаторов, используемых при проведении процессов изомеризации. [47]
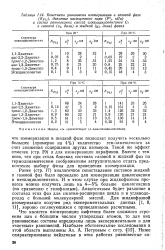 |
Константы равновесия изомеризации в газовой фазе. [48] |
Такой же эффект отмечен ( стр. Вместе с тем ясно, что при столь близких составах газовой и жидкой фаз по термодинамическим соображениям затруднительно отдать предпочтение выбору фазы для проведения изомеризации. [49]
Приведенные кинетические уравнения для необратимой и обратимой реакций первого порядка широко используются для изучения изомеризации при умеренных степенях превращения, когда с заметной скоростью протекают только одна-две стадии. Если изомеризация, протекающая в одну-две стадии, сопровождается побочными реакциями крекинга или гидрокрекинга ( причем все реакции подчиняются уравнению первого порядка), так - ке можно выполнять, интегрирование дифференциальных кинетических уравнений, но нужно учитывать условия проведения Изомеризации. [50]
Близко по своей природе к реакциям перегруппировок примыкают реакции изомеризации, например, многочисленные процессы изомеризации углеродов в присутствии галогенидов алюминия. Так, проведение изомеризации - бутана в изо-бутан с катализатором А1С13 в присутствии либо молекулярного трития, либо хлористого водорода, меченного тритием, показало, что в этой реакции важное участие принимает НС1, являющийся переносчиком водорода. [51]
Близко по своей природе к реакциям перегруппировок примыкают реакции изомеризации, например, многочисленные процессы изомеризации углеродов в присутствии галогенидов алюминия. Так, проведение изомеризации и-бутана в изо-бутан с катализатором А1С13 в присутствии либо молекулярного трития, либо хлористого водорода, меченного тритием, показало, что в этой реакции важное участие принимает НС1, являющийся переносчиком водорода. [52]
Таким образом, при алкилировании фенола изобутиленом получается довольно чистый параизомер с высоким выходом, который может непосредственно употребляться в различных органических синтезах. В моно-е / шр-бутилфеноле содержится до 50 % ортоизомера, на образование которого непроизводительно расходуется значительное количество олефина. Следовало выяснить возможность проведения изомеризации орто-бяшр-бутилфенола в параизомер, совместив этот процесс с основным производством получения алкилфенолов с применением одного катализатора. [53]
При применении катализаторов типа Фридель-Крафтса изомеризация парафинов, за исключением бутана, обычно сопровождается побочными реакциями, включающими и разрыв связи С-С. В процессе реакции синтезируются соединения, кипящие либо выше, либо ниже первоначального углеводорода. По аналогии с реакциями, происходящими в автодеструктивном алкилировании, описываемый процесс является все-таки соединением деалкилирования ( крекинг) и алкилирова-ния [410], которые дают изопарафины более высокого либо более низкого молекулярного веса, чем первоначальный алкан. Возможно, проведением изомеризации под давлением водорода [411 - 413], в присутствии изобутана [412, 414], ароматики [412], нафтеновых углеводородов [412, 415-418] или гетероциклических углеводородов, таких как тиофен [419], можно свести к минимуму боковые реакции для пентанов и гексанов, но не для геп-танов и более высоких парафинов. Устранение побочных реакций обычно сопровождается замедлением изомеризации, однако, прибавление олефинов уменьшает предохраняющее действие вышеприведенных агентов. [54]
При распаде соответствующего карбаниона затрагивается преимущественно асимметрический центр во входящем в азометиленовую систему остатке а-фенилэтил-амина. После того как изомеризация оптически активного соединения VII в системе трепг-бутилат калия - игрепг-бутиловый спирт - d при 75 прошла на 17 %, был проведен анализ возвратившегося исходного материала. Последний состоял на 57 % из продукта изотопного обмена и лишь на 3 % - из продукта рацемизации. Количество исходного продукта, регенерирующегося при распаде карбаниона ( при проведении изомеризации на 17 %), не настолько велико, чтобы существенно изменить эту величину. [55]
Для изомеризации практически чистых я-бутана и я-пентана, характеризующейся слабой экзотермичностью при глубоких кон-версиях и отсутствии гидрокрекинга, значения ДГад не превышают 20 - 25 С. Такое увеличен-ие температуры в одном реакторе вполне допустимо. Если часть сырья подвергается гидрокрекингу ( сильно экзотермический процесс), то АГад возрастает и достигает 34 - 42 С при гидрокрекинге 5 % сырья. Такое повышение температуры нежелательно и может ухудшить селективность основного процесса. Поэтому проведение изомеризации я-бутана или я-пентана в единичном реакторе возможно, если гидрокрекингу подвергается не более 1 - 2 % сырья. [56]
Страницы: 1 2 3 4